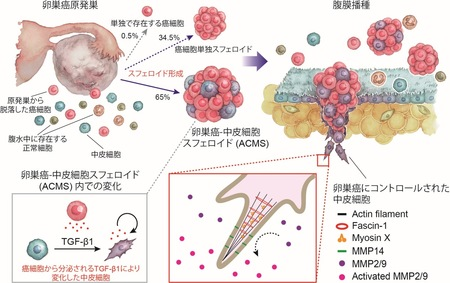
名古屋大学大学院医学系研究科産婦人科学の梶山 広明教授、宇野枢客員研究者らの研究グループは、卵巣がん-中皮細胞スフェロイドという腹水中の構造形成が、卵巣がんの特徴である急速な腹膜播種形成に重要となるメカニズムを発見した。
同研究では、なぜ卵巣癌を早期発見することが難しいのかという臨床的疑問を、最新の遺伝学的解析と顕微鏡技術、マウスモデルを用いて検討した。これまでは、発生部位である卵管・卵巣から腹腔内に脱落した卵巣がん細胞は、単独で腹水中に存在していると考えられていたが、同研究では、豊富な臨床腹水検体を用いて、卵巣がん細胞が単独ではなく、複数の細胞が集合するスフェロイドという特徴的な構造で生存していることを示した。
また、そのスフェロイドが、実際には卵巣がん細胞単独ではなく、腹腔内の最も重要な正常細胞の一つである中皮細胞とスフェロイドを形成していることを、最新の顕微鏡技術と特殊なマウスモデルを用いて明らかにした。
この卵巣がん-中皮細胞スフェロイド(ACMS)は、卵巣がん単独のスフェロイドと比較して、腹腔内条件で生存率が高く、通常の抗がん剤に対しても抵抗性が高く、また腹膜表面への浸潤能が非常に高いことを、連続撮影で可視化することに成功した。
卵巣がん-中皮細胞スフェロイド(ACMS)形成を通して、卵巣がんからのTGF-β1を中心としたシグナルにより、中皮細胞に劇的な変化が生じる一方で、卵巣がん自体には大きな変化が起きていないことが判った。
卵巣がんにコントロールされた中皮細胞はFascin-1などの浸潤に関与するタンパク発現を増加させて組織に積極的に浸潤し、卵巣がんは中皮細胞が形成した経路を利用することで早期に、さらに容易に腹膜播種を形成できることを明らかにした。
同研究成果により、卵巣がん細胞と正常細胞との関わりの重要性が認識され、卵巣がんの早期播種形成のメカニズムの解明や新たな治療アプローチ再考の必要性、さらには卵巣がん再発のメカニズム解明につながるものと期待される。これらの研究成果は、2月6日付で国際科学総合雑誌「Science Advances」に掲載された。
卵巣がんは、早期発見が非常に難しく、3ヵ月ごとの超音波検査や腫瘍マーカー採血検査を行ったとしても早期に診断することは困難であり、卵巣がんのスクリーニング方法は確立されていない。
また、初期には症状が乏しいため、卵巣がん患者の約70%は、腹腔内に多量に播種病巣と腹水が存在する進行期で発見される。そのため、卵巣がんはサイレントキラーとも呼ばれる最も予後の悪い婦人科がんだ。
これまで、卵巣がんがなぜ短期間に急速に腹腔内播種を形成できるのかは分かっていなかった。他がん種と比較して、卵巣がんは腹膜播種という特徴的な転移様式にて、お腹の中に多くの転移を形成する。これは、他がん種が血中やリンパ管を通して転移をきたすのとは異なり、腹腔内に脱落した卵巣がん細胞が、腹水中で生存し、その腹水を利用して腹腔内に生着することを意味する。
また、過去の研究の多くは、腹水中の細胞成分を、他の組織と同様に扱っていたため、特殊な腹腔内環境を十分に説明できておらず、正確な細胞構成も明らかになっていなかった。
同研究では、この腹水中に存在する卵巣がん細胞が、どのようにして腹水中で生存することができ、腹膜播種を早期に形成できるのかについて、多くの臨床検体と特殊なマウスモデルを、最新の顕微鏡技術と遺伝解析技術を用いて次の5つの点が明らかにされた。
① 卵巣がんは腹水中でスフェロイドという細胞集合体として生存している。
② 腹水中には中皮細胞が最も多く存在する間質細胞である。
③ 卵巣がん細胞は中皮細胞と癌―中皮細胞スフェロイド(ACMS)を形成している。
④ ACMSは卵巣がん単独のスフェロイドよりも非常に高い浸潤能を持っている。
⑤ ACMS形成を通して、卵巣癌細胞は中皮細胞の性質を劇的に変化させることができ、変化した中皮細胞が高い浸潤能を獲得し、卵巣癌はその経路を辿るだけで播種形成を行える。
①~⑤の各詳細は、次の通り。
① 卵巣癌は腹水中でスフェロイドという細胞集合体として生存している。
実際の患者の腹水検体の観察を通して、卵巣がんのほぼ99%はスフェロイドという細胞集塊を形成していることを確認した。この構造は検体により多様な構造を示しており、単独の卵巣がん細胞はほぼ確認できなかった(図2)。
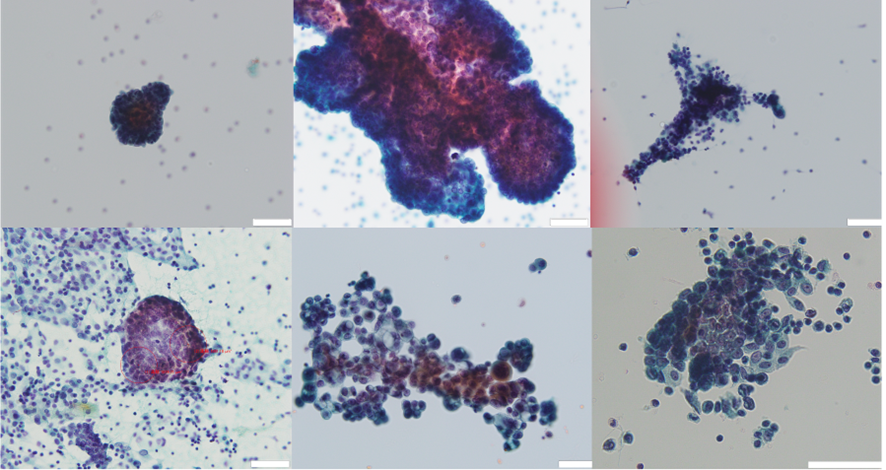
図2. 腹水中に存在する卵巣がん細胞の形態。ほぼ全ての細胞が細胞集塊であるスフェロイドという構造を形成している。大きさや形は検体によって多様である。スケールバー:50μm
② 腹水中には中皮細胞が最も多く存在する間質細胞である。
がん細胞スフェロイドの周囲には、単独の正常細胞が多く存在している。その細胞構成を、病理学的な形態的評価と、single-cell RNA sequencing解析のデータを用いて、詳細に評価した。
その結果、これまで腹水中に多く存在するとされていた間質細胞である線維芽細胞(fibroblast)のほとんどが、実際には中皮細胞で形成されていることが判った(図3)。この結果は、過去の報告で線維芽細胞とされていた細胞の性質が、実は中皮細胞についての性質であった可能性を示唆しており、がんが発生する部位によって、構成細胞を入念に検討する必要があることを示している。
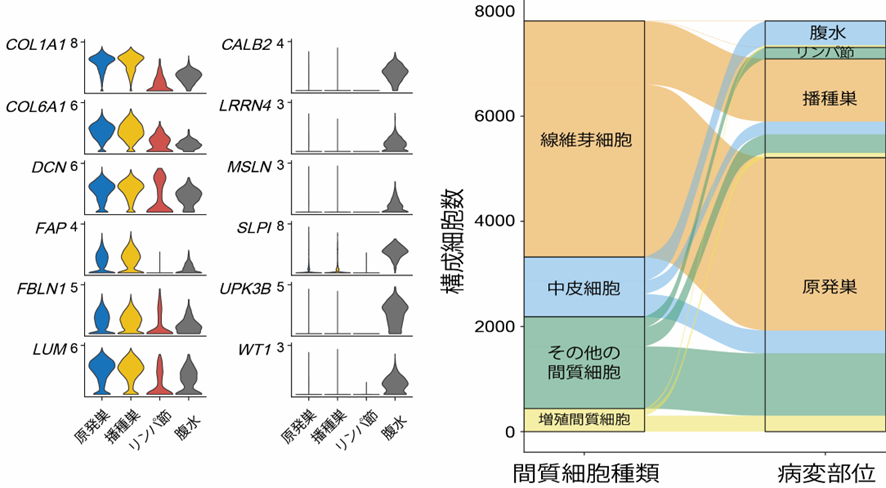
図3 原発(Primary)、播種(Metastatic)、リンパ節(Lymph Node)、腹水(Ascites)における正常間質細胞の分布をsingle-cell RNA sequencing解析で示した図。左図は線維芽細胞(Fibroblast)マーカー、中央は中皮細胞(Mesothelial cell)マーカーを発現する細胞を示す。腹水中の細胞は中皮細胞マーカーを多く発現していることを示している。右図は各細胞がそれぞれの組織で構成する細胞を示し、水色の中皮細胞(Mesothelial cells)が腹水(Ascites)の最も重要な間質細胞であることを示す。
③ 卵巣癌細胞は中皮細胞と癌―中皮細胞スフェロイド(ACMS)を形成している。
スフェロイドの詳細な観察により、多くのスフェロイドでは、卵巣がん細胞のみではなく、中皮細胞様の細胞も卵巣がんスフェロイドに含まれていることが分かった。この卵巣がんスフェロイドの構造を明らかにする目的で、内部まで立体的に観察できる最新の顕微鏡技術である多光子顕微鏡を用いてスフェロイド全体を観察した結果、60%以上のがんスフェロイドには中皮細胞が含まれていることを明らかにた(図4)。
また、この中皮細胞の割合は、抗がん剤使用後の検体で著明に増加していた(図5)。
さらに、中皮細胞を赤色に標識できるようにした特殊なマウスモデルを用いて行った実験でも、緑色に染色したがん細胞は、赤色の中皮細胞とスフェロイドを形成していることが明らかになった。
これらの結果を踏まえ、この卵巣がん細胞―中皮細胞スフェロイドを新たにAggregated Cancer-Mesothelial Spheroid (ACMS)と定義した。
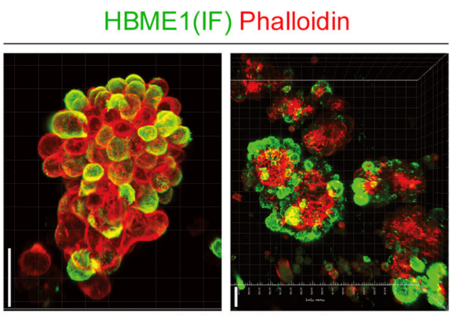
図4 卵巣癌-中皮細胞スフェロイドの代表的な図。緑色は中皮細胞を標識するHBME1染色陽性の中皮細胞、赤色はがん細胞スフェロイドの全体像を示す染色。卵巣がんスフェロイドは、卵巣がん単独ではなく、中皮細胞が含まれていることを多光子顕微鏡という高度な顕微鏡で確認した。スケールバー:50㎛
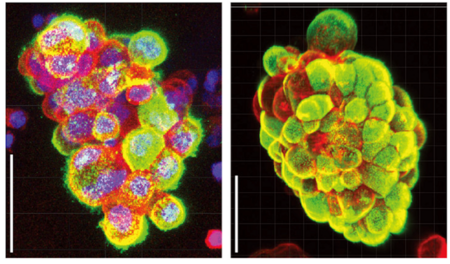
図5 抗癌剤使用後の卵巣がん-中皮細胞スフェロイドの形態変化図。図4と比較して卵巣がんスフェロイドに占める中皮細胞の割合が増加しており、このようなスフェロイドは抗がん剤耐性を持っていることを示唆する所見である。スケールバー:50μm
④ ACMSは卵巣癌単独のスフェロイドよりも非常に高い浸潤能を持っている
続いて、なぜ卵巣がん細胞は中皮細胞とスフェロイドを形成する必要があるのかについての検討を行った。その結果、がん細胞―中皮細胞スフェロイド(ACMS)は、卵巣がん細胞単独のスフェロイドと比較して、腹水中での生存率が高く、抗がん剤に対して抵抗性を持ち、さらに周囲の組織への浸潤能が高いことが分かった。
ACMSからどのように他臓器へ浸潤を行うかを、継時的な撮影で詳細に観察したところ、常に中皮細胞が先に周囲へ浸潤し、卵巣がん細胞はその後を追うように、組織へ浸潤している所見を確認した(図6)。
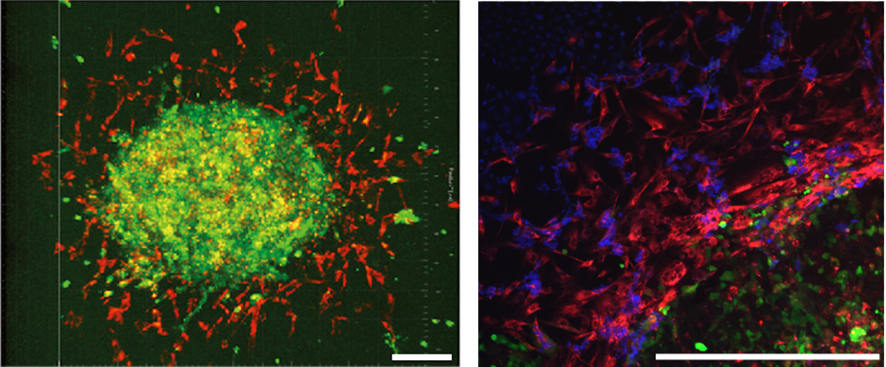
図6 卵巣がん―中皮細胞スフェロイド(ACMS)から中皮細胞が周囲の組織へ浸潤する図。卵巣がん細胞は緑色、中皮細胞は赤色に標識している。左図は赤色の中皮細胞が周囲のコラーゲン組織へ積極的に浸潤し、緑色の卵巣癌細胞はその後ろを追ってくる所見を示す。右図は正常腹膜中皮細胞(青色)へ、スフェロイドを形成していた中皮細胞(赤色)が先に浸潤をしている所見である。緑色の卵巣がん細胞はまだ内部にとどまっているため、卵巣がん細胞単独のスフェロイドではほとんど浸潤を示さない。スケールバー:200㎛
⑤ ACMS形成を通して、卵巣癌細胞は中皮細胞の性質を劇的に変化させることができ、変化した中皮細胞が高い浸潤能を獲得し、卵巣癌はその経路を辿るだけで播種形成を行える。
卵巣がん細胞―中皮細胞スフェロイド(ACMS)内で、卵巣がん細胞と中皮細胞にどのような遺伝子発現の変化が起こっているのかを確認したところ、卵巣がん細胞での遺伝子発現変化はわずかであった。
一方で、中皮細胞には劇的な変化が起こっていることを確認した。その中で、特にTGF-β1経路が上昇しており、その結果、中皮細胞での浸潤に寄与するタンパクであるFascin-1やMMP2/9などが上昇していることが判った。
卵巣がんとの接触を受けて、性質が大きく変わった中皮細胞は高い浸潤能を持つことを示した(図7)。その結果、卵巣がん細胞はACMS形成を通して中皮細胞を巧みにコントロールし、転移の足掛かりを形成させ、卵巣がん細胞自身は大きく変化することなく、短期間に広範な腹膜播種を形成できることを示した(図1)。
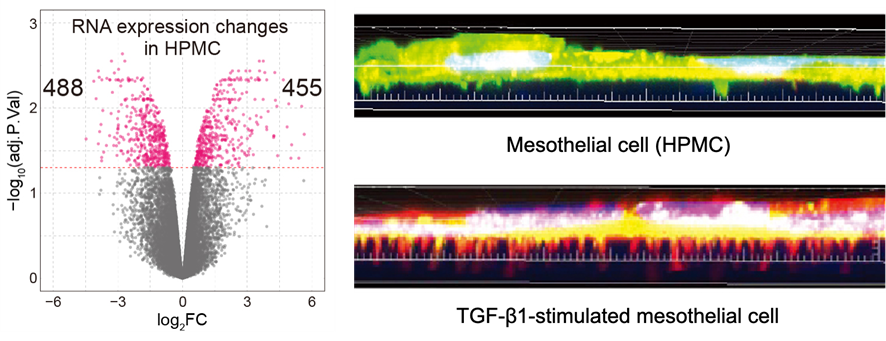
図7 卵巣がん細胞とのスフェロイド形成を通して中皮細胞は遺伝子発現を劇的に変化させる(左図)。主な経路であるTGF-β1刺激により、浸潤に関与するスパイク状のinvadopodiaと呼ばれる構造が増加する(右図)。
これらの研究成果は、卵巣がんの本質に関わる部分を明らかにすることができたとともに、卵巣がん細胞―中皮細胞スフェロイド(ACMS)の強固な結合は、抗がん剤耐性の原因と考えられる。このACMSにおける治療抵抗性をさらに検討することで、今後の治療戦略や高い再発率のメカニズム解明の足掛かりになる可能性がある。
また卵巣がんに対するカルボプラチン腹腔内投与が今般、日本で薬事承認・保険適用となり、日常臨床において腹腔内ポートを通じた腹水へのアクセスが可能となった。
腹腔内への薬剤投与に際して、経時的な腹水細胞診に加えてACMSの存在や質を評価することは、治療効果推定のバイオマーカーや治療抵抗性の鍵となる可能性がある。今後、腹腔内温熱化学療法(HIPEC)など、ACMSを標的とした補助治療により、前述したカルボプラチンなどの通常の抗がん剤の効果をより増強させることで腹膜播種の予後改善が見込まれる。
また、腹膜播種をきたす他領域のがん種(胃癌、大腸癌、膵癌など)へも応用できる可能性があり、同研究をさらなる発展により、治療応用へ繋がりが期待される。


