ブリストルマイヤーズスクイブ(BMS)は17日、経口投与可能な選択的チロシンキナーゼ2(TYK2)阻害剤「ソーティクツ」について、米国FDAが活動性乾癬性関節炎(PsA)を有する成人患者の治療薬として承認したと発表した。同剤は、PsAに対して承認された初めてのTYK2阻害剤となる。
今回のFDAの承認は、活動性PsAを有する成人患者におけるソーティクツ6mg を1日1回経口投与の有効性および安全性を評価したピボタルなPOETYK PsA-1試験およびPOETYK PsA-2試験の良好な結果に基づくもの。
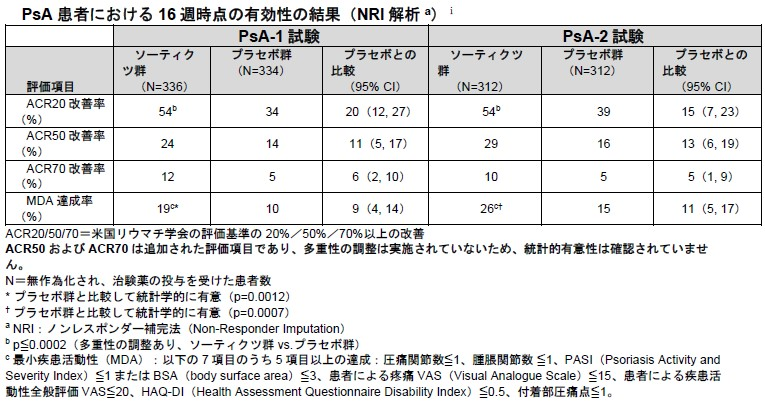
両試験で、ソーティクツによる治療は、ACR20 改善率(主要評価項目)および最小疾患活動性(MDA)達成率(副次評価項目)の評価指標において、疾患活動性を有意に改善した。
活動性PsA患者におけるソーティクツの安全性プロファイルは、尋常性乾癬患者における安全性プロファイルと概ね一致していた。最も多く認められた(ソーティクツ群の1%以上に発現し、プラセボ群に比べて高頻度に発現)した有害事象は、上気道感染、血中クレアチンホスホキナーゼ増加、単純ヘルペス、口内炎、毛包炎およびざ瘡であった。
ソーティクツには、過敏症反応、感染症、結核、悪性腫瘍(リンパ腫を含む)、横紋筋融解症およびCPK上昇、臨床検査値異常、予防接種ならびにJAK阻害に関連する潜在的リスクについての警告および注意喚起が関連付けられている。
ソーティクツは、全身療法または光線療法の候補となる中等症から重症の尋常性乾癬成人患者の治療薬として、2022年に初めてFDAの承認を取得した。
同適応において、ソーティクツを他の強力な免疫抑制剤との併用は推奨されていない。FDAの承認取得後、ソーティクツは同適応で世界各国の規制当局の承認を取得している。
ソーティクツは、中等症から重症の尋常性乾癬患者を対象とした5年間の実臨床における有効性および安全性データを有している。
◆プロビデンス・スウェーデン医療センターリウマチ学研究責任者のPhilip J. Mease氏(ワシントン大学医学部の臨床教授、M.D.)のコメント
PsAは、関節症状および皮膚症状の両方を伴う慢性的かつ進行性の自己免疫疾患である。関節、腱または靭帯に痛みを伴い、日常生活の動作や活動に支障をきたす場合もあり、有効な新規経口治療薬が必要とされている。
臨床試験では、36-Item Short Form Health Survey(SF-36)を用いて健康関連QOLを測定した。16週時点において、ソーティクツ群では、プラセボ群と比較して、SF-36の身体的側面のサマリー(PCS)スコアで改善が示され(主な副次評価項目)。
また、SF-36 PCSの4つのドメイン(身体機能、日常役割機能(身体)、体の痛み、全体的健康感)のすべてのスコアでも改善が認められた。ソーティクツは症状管理を通じて、患者さんに大きなな変化をもたらす可能性がある。
◆Al Reba BMS心血管・免疫疾患領域コマーシャリゼーション部門シニアバイスプレジデントのコメント
本日の発表は、活動性PsAを有する成人患者さんに、差別化された新たな治療選択肢をもたらすものだ。
今回の承認は、乾癬性疾患の皮膚および関節症状の管理においてソーティクツが果たす重要な役割を裏付けるものであり、限られた治療選択肢しかない疾患、あるいは治療選択肢がない疾患に対して治療薬を開発し続ける当社の取り組みにおいても重要なマイルストーンとなる。


