がん転移抑制剤への応用に期待
岐阜大学応用生物科学部山内恒生助教のグループは13日、代表的なフラボノイドであるケルセチンとその誘導体のがん転移抑制機構の一端を、標的タンパク質の結合様式を調査することにより明らかにしたと発表した。
5種類のフラボノイドプローブを新たに合成し、これを使ったプルダウンアッセイにより、ケルセチン誘導体の標的タンパク質としてMMP-1を同定した。ケルセチンおよびその誘導体(3MQ)は、MMP-1を阻害した。MMP-1は抗癌細の転移に関わるため、ケルセチン誘導体のがん転移抑制剤としての応用が期待される。
また、表面プラズモン共鳴(SPR)法により、ケルセチン誘導体とMMP-1 触媒ドメインとの濃度依存的な相互作用が示した。
さらに、核磁気共鳴分光 (NMR) 法により、3MQはMMP-1の金属イオン周辺と相互作用することが判明した(図1)。
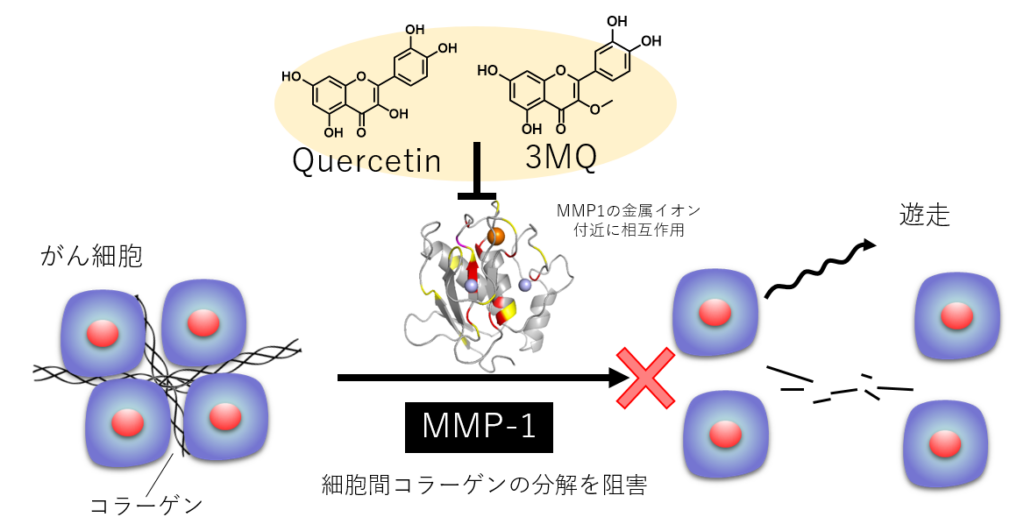
フラボノイドプローブの開発により、新たな標的タンパク質発見の可能性が広がり、フラボノイドの多様な生理活性の中核的なメカニズムの解明が注目されている。これらの研究成果は、6日にBioorganic & Medicinal Chemistry誌のオンライン版で発表された。
がんは、細胞の異常増殖と転移を特徴とする疾病である。がんの進行は4つの段階で起こる。このうち「転移」は、がん細胞の移動により、がんが発生した場所から体のさまざまな部位に広がっていく段階である。
そのため転移の抑制はがんの治療において重要であり、これまでに細胞運動の促進に関連する遺伝子、酵素、リガンド、細胞内シグナルがいくつか報告されている。
フラボノイドは、植物に含まれる二次代謝物の一種で、C6-3-6骨格を有している。フラボノイドの薬効については多くの研究がなされており、抗酸化作用、抗炎症作用、抗がん作用など幅広い生理作用を示すことが報告されている。
ケルセチンには、抗酸化作用、メラニン生成抑制作用、抗腫瘍作用など、さまざまな生理活性があり、多くの研究で示されている。加えて、いくつかのタンパク質がケルセチンの標的となると報告されている。
以前の研究で、ケルセチン誘導体が皮膚がん、及び卵巣がん細胞において抗遊走および抗浸潤活性を示すことが明らかにされている。
また、ケルセチンは、マウスの体内での転移抑制作用も報告されている。だが、ケルセチン及びその誘導体の抗遊走、抗浸潤、抗転移活性の分子機構は、20年以上にわたって解明されていなかった。
そこで、山内氏らは、ケルセチン誘導体の標的タンパク質を、プルダウンアッセイを用いて調査し、ケルセチン誘導体との作用機序をNMRやSPR法を用いて調査した。
研究では、フラボノイドの特定の水酸基にキャリアビーズを結合させ、標的タンパク質を決定するプルダウン法に用いるフラボノイドプローブの新しい合成法の開発に成功。同プローブを用いてケルセチン誘導体の標的タンパク質を明らかにし、その作用様式をタンパク質のNMR測定により明らかにした。
フラボノイド誘導体にBorax、Benzyl、acetoglucose保護でアミノエトキシ基を特異的に導入し、5種類のフラボノイドプローブを作製した(図2)。
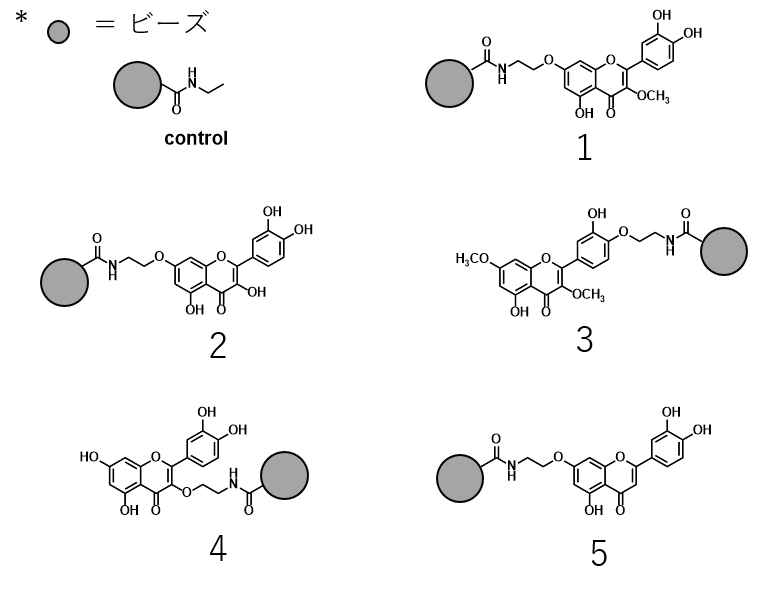
合成したフラボノイドプローブを用いたプルダウンアッセイにより、MMP-1がケルセチン誘導体の標的タンパク質の一つであることが示唆された。
次に、ケルセチン誘導体とMMP-1の結合様式をSPRおよびHSQC分析により検討した。SPR解析では、ケルセチン誘導体とリコンビナントMMP-1触媒ドメインの相互作用は濃度依存的であることが確認された。
また、結合の強さを示すKd値を算出したところ、3MQはケルセチンよりも強力にMMP-1と結合していることが明らかになった。
MMP-1阻害活性及び、がん細胞遊走阻害活性がケルセチンよりも3MQの方が強いため、このSPRの結果はこれらの結果を支持していた。15N標識したMMP-1触媒ドメインを用いた1H-15N HSQC NMR解析により、3MQはZn2+イオンだけでなく、Ca2+イオンも含むすべての金属イオン付近と相互作用していることが示された(図3)。 これらの結果から、ケルセチン誘導体は、金属イオン付近に結合してMMP-1の活性を阻害し、がん細胞の遊走を抑制しているのではないかと考察された。
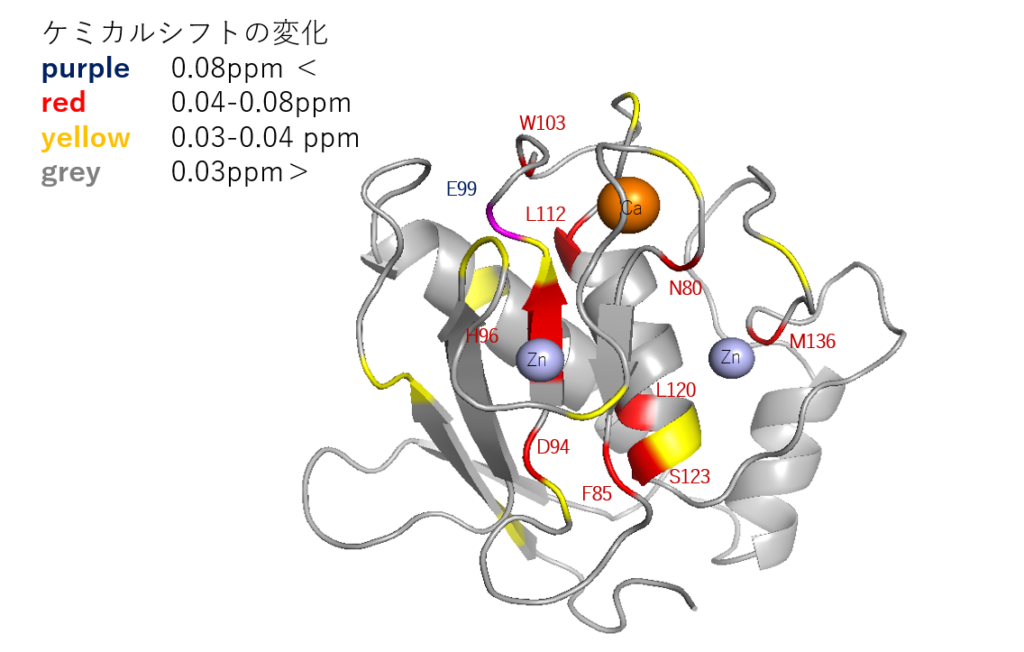
ケルセチンは、玉ねぎや柑橘類など植物中に多く含まれており、抗炎症や高肥満、抗がん活性など様々な生物活性が報告されている。
ところが、その作用メカニズムは十分に明らかにされていない。フラボノイドプローブの開発と結合様式の解明は、新たな標的タンパク質発見の可能性を広げ、フラボノイドの多面的な生理活性の中核となるメカニズムを明らかにすることができるのではないかと期待される。
また、ケルセチン誘導体のがん転移阻害の標的タンパク質の一つをMMP-1であることが示唆されたため、今後、MMP-1を阻害する新たな化合物の探索が注視される。


