
相澤病院臨床検査センターエコーセンター センター長/循環器内科顧問の安河内聰氏は、バイエル薬品プレスセミナーにおいて、「小児の血栓症予防に患者負担の少ない新たな選択肢―フォンタン手術後の血栓症予防の現状と課題―」をテーマに講演した。元日本小児循環器学会理事長として小児循環器治療の発展に貢献してきた同氏が、フォンタン手術、フォンタン術後の血液凝固異常、血栓予防と治療の実際、新しい抗凝固薬としての「イグザレルト」の役割、日本における小児用医薬品開発の未来について解説した講演内容を紹介したい。
フォンタン手術とは?
フォンタン手術はチアノーゼ(血液中の酸素濃度が低い状態)を示す先天性心疾患に対する修復術の一つである。最初のフォンタン手術は 1971 年、今から 50 年以上前に右心房と右心室の間の弁が先天的に閉じている三尖弁閉鎖に対して行われている。
心臓には、肺に血液を送る右心室と全身に血液を送る左心室の二心室があり、二つのポンプによって血液が循環している。
だが、先天性心疾患の患者の中には右心室だけ、もしくは左心室だけ、つまり一つのポンプで全身の循環を賄わなければならない単心室循環の人がいる。フォンタン手術の対象となる先天性心疾患は、三尖弁閉鎖、左心低形成症候群、単心室、左右心室不均衡の房室中隔欠損、多発性心室中隔欠損、房室弁交叉などである。
正常な二心室循環では、酸素濃度の低い静脈血と酸素濃度の高い動脈血が分かれているため、チアノーゼはない。だが、単心室循環では静脈血と動脈血が混ざって全身へ流れていくため、全身の血液の酸素濃度が下がりチアノーゼが生じる。
フォンタン手術は単心室循環に対して機能的にチアノーゼを取ること(酸素化)を目的として、全身から心臓に戻ってくる上大静脈と下大静脈を直接、肺動脈につなぐ手術である。単心室循環を二心室循環にするのではなく、血流を改善する。術後は、静脈血が肺に流れ、肺からの動脈血だけが心臓に戻り全身に流れるようになるため、静脈血と動脈血が混ざらなくなりチアノーゼが取れる。
術式はいくつかあるが、現在ほとんどの施設は、心臓の外側に置いた人工血管で下大静脈を肺動脈につなぐ「心外導管型」を行っている。
日本循環器学会のレジストリデータによると、日本では先天性心疾患の手術件数は年間約9000件、そのうちフォンタン手術は 400 件程度である。10年間で4000人なので、決して数は多くはないが、ものすごく珍しいわけでもない。
正常な二心室循環では、左心室から駆出された血液は大動脈を通して全身に流れる。心臓に戻ってくると右心房でかなり低い血圧になり、右心室というポンプを使って肺動脈に押し込められ、肺循環を回り心臓に戻ってくる。
二つのポンプがそれぞれ機能しているわけだ。だが、フォンタン循環(単心室循環)の場合はポンプが一つしかなく、全身から戻ってきた血液はそのまま肺動脈に流れ、駆出される。このため、フォンタン循環の特徴(図1)として、高い中心静脈圧が挙げられる。

通常、中心静脈圧は平均5mmHgであるが、フォンタン循環では10~15mmHg と2倍から3倍高くなる。また、体心室(全身に血液を送り出す心室)が一つしかないため、体心室の機能異常を起こしやすくなる。
心臓が血液を送る力が弱く、心拍出量は二心室循環の70%程度だ。また、非拍動性の血流が肺動脈に流れるため、運動対応能が低下する。個人差があり、野球やサッカーをする人もいるが、全般的には健常な人に比べ運動対応能が低下することが特徴である。
これらの特徴から、フォンタン術後は多臓器の異常を生じることが知られている。心臓に関してはチアノーゼが残ったり、不整脈を起こしやすかったりする。また、中心静脈圧が高いため、肝うっ血が続くことにより肝線維症、肝硬変、肝細胞がんなどの肝機能異常や、慢性腎不全などの腎機能異常を起こしやすく、血液異常では血栓症、血液凝固異常を起こしやすいことが問題になる。
フォンタン術後の血液凝固異常
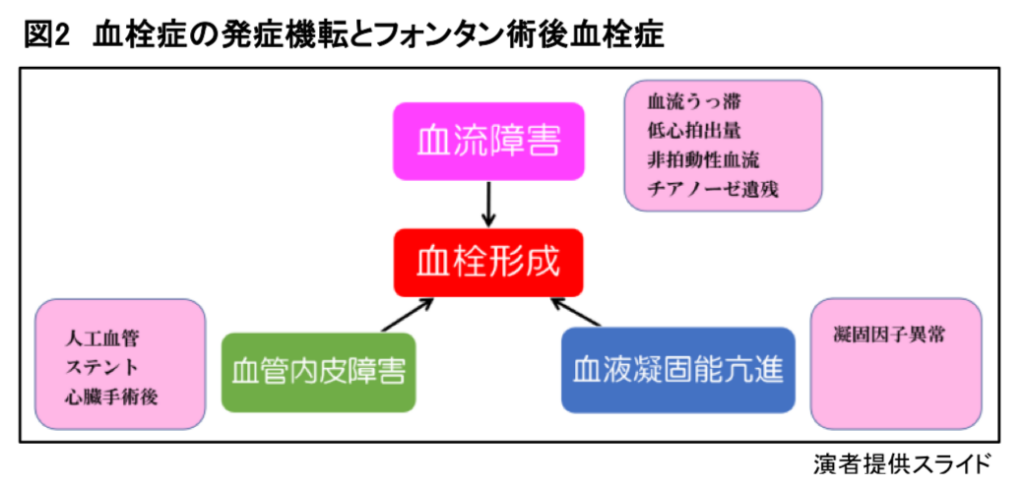
血栓症の発症機転となる血流障害、血管内皮障害、血液凝固能亢進があると、血栓が形成されやすくなる(図2)。フォンタン循環では血流がうっ滞しやすく、非拍動性でダラダラ流れるため、血栓ができやすくなる。
血管内皮障害としては、心外導管型手術で用いられる人工血管や肺動脈に留置されたステントなどの人工の異物があるため、血栓ができやすくなる。さらに、フォンタン術後の方は血液凝固能異常を生じており、さらに血栓を生じやすくなる。
フォンタン術後の血栓症の発生率は 17~33%といわれている。術後6カ月以内に多く、その後いったん低下するものの、術後2 年ぐらい経過すると再度増加するという特徴がある。また、心房頻拍、心房細動、心房粗動などの心房性不整脈を合併した人や、右心耳と肺動脈を直接つなぐ手術をした人に血栓が起きやすいと報告されている。
フォンタン術後の血栓予防と治療の実際
フォンタン術後の抗凝固療法/抗血栓療法については、抗凝固薬のワルファリンと抗血小板薬のアスピリンが従来使われてきた。術後早期はワルファリンが使用されるが、その後、だんだんとアスピリンに切り替えられ、術後15 年経つとワルファリンはあまり使われなくなるという報告がある。
ただ、フォンタン術後の抗凝固療法のプロトコルには施設間差があり、どの薬をどのように使うべきか明確に決まっておらず、ワルファリン単剤、アスピリン単剤、両剤を使う施設もあれば、何も使っていない施設もある。
アメリカ心臓協会(AHA)が2019年に出したステートメントでは、フォンタン術後患者は血栓症のリスクがあり、血栓予防法は確定していないが抗血小板療法または抗凝固療法が推奨されるワルファリンとアスピリンの優劣は未確定で、DOACについては今後考慮すべき課題だと述べられている。
ワルファリンは、投与量が多すぎると出血しやすくなり、不足すると血栓のリスクが高くなるため定期的な採血による血液凝固能のモニタリングが必要で、1~2カ月に1度、病院に行って針を刺して採血しなければならない。
また、ワルファリンには顆粒があるものの小児用製剤はない。フォンタン術後の血栓症と出血の発生率を期間別に見ると、術後1年以内は血栓症がメインである。フォンタン手術を行うのが3歳頃だとして、術後1~5年後、小学生の頃に血栓症よりも今度は出血の頻度が高くなる。
術後5~10 年後の中学・高校生では出血が主な問題になってくる。さらに15 年以上経つと、血栓症も出血も増えるが、やはり出血が主になってくる。従って、血栓症の予防だけではなく、出血のリスクを考えなければならない。
フォンタン術後の抗凝固療法/抗血栓療法では、血栓予防と出血予防の微妙なバランスを保つことが重要である。成長発達に伴う凝固能の変化、生活環境・様式の変化、食生活の変化、フォンタン循環動態の変化、合併症・遺残症などについても考慮しなければならない。小児で使用できるワルファリン、アスピリン以外の第3の抗血栓薬という選択肢が増えることはより安全に抗血栓療法を行う上で重要であり、この意味でリバーロキサバンが新たな選択肢として承認を受けたことは非常に大きなインパクトだと思われる。
リバーロキサバンは、納豆の摂取に問題なく、定期的な採血の必要はない。小児用製剤もある。腎機能については注意が必要であるが、フォンタン術後の抗血栓療法の第3の選択肢になり得ると考えている。
UNIVERSE STUDY から学ぶこと
UNIVERSE STUDYは、組み入れ4カ月以内に最初のフォンタン手術を完了している2~8歳の機能的単心室症を有する小児患者を対象とした国際共同P3試験である。パートAが薬理学的評価で12 例、パートBが安全性・有効性評価で 100例である。日本人の組み入れ症例数はパートB に9例で、うち1例が対照のアスピリン群に入っている。
リバーロキサバンは小児でも服薬しやすいドライシロップの剤形で1日2回服薬し、用量も体重別に7~8kg、8~10kg、10~12kg、12~20kg、20~30kgと細かく設定されている。治験の結果としては、フォンタン術後血栓抑制におけるリバーロキサバンの有効性および安全性が示された。
本国際共同治験においては日本小児循環器学会臨床治験委員会の企業治験サポート体制により、治験研究責任者(PI)の選定や治験グループ(治験施設と施設責任者)の構成、レジストリデータの利用などの支援を受けている。小児治験ネットワークを活用して、症例組み入れ期間内に予定症例数を超える8例(リバーロキサバン群)の登録が終了した。

リバーロキサバンによるフォンタン術後の抗凝固療法の臨床的位置付けを考えると、その利点として「経口投与」、「小児用のドライシロップ製剤がある」、小児の薬用量が細かく設定されている」、「血液凝固能のモニタリングが不要なため定期的な採血が不要」、「風邪などによる食事摂取の制限や下痢・嘔吐などによる影響が少なく、入院管理による投与量の調節が不要」ーが挙げられる。
課題は、使用経験がまだ少ないことであるが、これから経験が増えれば、より適正な使用になってくると思われる。残念ながら現在は、成人のフォンタン術後患者は保険適用外となっている(図3)。
本邦における小児医薬品開発の課題
日本の小児薬物治療には、添付文書に小児についての用法・用量が明記されていないにもかかわらず、小児に投与されている現実がある。その多くは適応外薬や小児使用についての未承認薬が多く、十分な安全性・有効性が確認されずに使用されている場合が多いのが現状である。
何か医療的な問題が起こったときに、使用したドクターの責任が問われることになるし、患者さんに対して救済の制度が使えないことが問題になってくる。
また、成人で開発され、小児に使用される可能性がある薬物でも、小児での開発が進まない現状もある。小児薬物開発・治験が難しい理由には、「対象症例数が少ない」、「対象症例年齢が新生児から思春期と幅広く成長発達による変化のバリエーションが多すぎる(対象とする疾患が多様で一つに絞りにくい)」、「開発投資に見合うリターンが少なく企業利益が生み出せない」などがある。
莫大な治験費用が必要となり、使用用量に応じた保険請求(薬価)では投資回収が難しく、さらに莫大な市販後調査の費用も生じてくる。投資回収が困難だと、企業としてもなかなか足を踏み込むことが難しい。
今回の小児治験がうまくいった理由は、まず、「企業の小児治験への強い意欲があった」、「成人での先行治験の延長線上の企画であった」、「学会の治験支援事業(図4)と連携できた」、さらに、「症例の組み込みにおいて小児治験ネットワークを活用できた」からである。
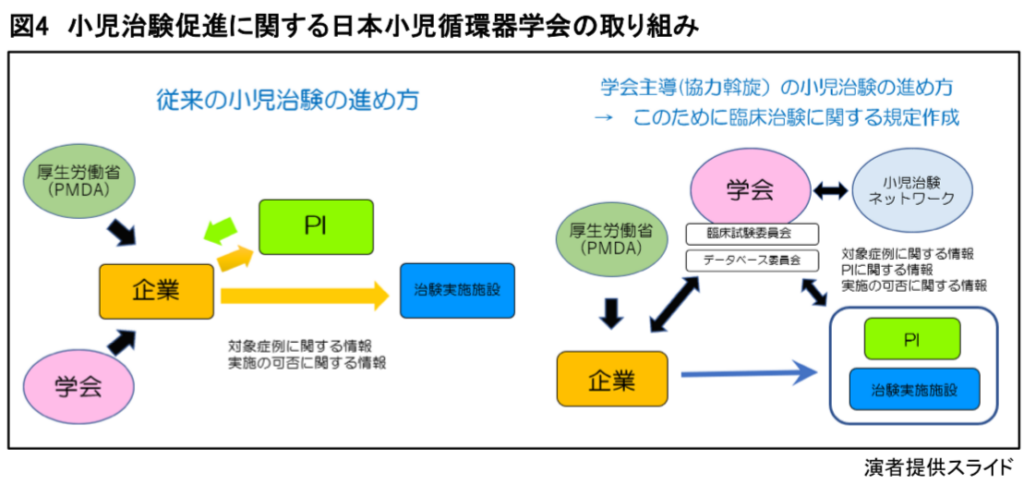
従来の治験の進め方では、企業が一生懸命PIを探し、治験グループを構成するため、準備に多くの時間と準備費用が必要であった。
一方、今回の治験のように学会支援制度を利用すると学会が症例の組み入れやPI の推薦、治験グループの構成について提案し、サポートしてくれる。症例の組み入れに関しても、必要に応じて全国に37施設ある小児治験ネットワーク参加医療機関を含めて、学会から所属会員に対して呼び掛けることができる。
2024年1月、厚労省から通達「成人を対象とした医薬品の開発期間中に行う小児用医薬品の開発計画の策定について」が出た。成人を対象とした医薬品の開発を行う場合、小児用医薬品の開発計画を策定し、成人を対象とした医薬品の承認申請を行うまでに開発を進めることが望ましいという内容である。
これは、非常に画期的で、企業の開発の強い後押しになる。アメリカでは一部で小児用医薬品の開発を義務付ける法律もある。今まで日本にはなかったこのような制度が少しずつ整備されてきている背景には、できる限りTherapeutic Orphan(治療における見捨てられた領域)を解消し、小児により安全で有効なよい薬を使ってもらいたいという国の考えもあると思われる。
フォンタン術後の血栓・塞栓症は、長期にわたる合併症であり、従来のワルファリンやアスピリンと同様の効果が期待されるリバーロキサバンは、治療の選択肢を増やすことができるという点で有用である。採血が不要なため、小児患者にとってより優しい医療が期待できる。
小児におけるTherapeutic Orphanやドラッグロスをなくすためには、産官学の連携による開発が必要で、今回のような治験促進方法が積極的に導入されて、よりよい薬を必要としている子どもたちに届けられる制度ができることを切に願っている。
【Take Home Message】
◆フォンタン術後の血栓・塞栓症は、フォンタン手術による血行動態や凝固因子異常などによって生じる長期にわたる 合併症である。
◆新しく本疾患の小児適応を取得した「リバーロキサバン」は、従来のワルファリンやアスピリンと同様の効果が期待され、治療の選択肢を増やすことができる。
◆「リバーロキサバン」は採血などのモニタリングが不要のため、小児患者にとってより優しい医療が期待できる。
◆小児における「Therapeutic Orphan」「ドラッグロス」をなくすためには、「産-官-学」の連携による小児医薬品・医療 機器の開発が重要である。


