ブタを利用した臓器異種移植への応用に期待
東京慈恵会医科大学腎臓・高血圧内科 横尾隆教授らの研究グループと大日本住友製薬は1日、共同研究でブタ腎臓の移植手術は胎仔の腎臓を用いれば拒絶反応が弱くなることを世界で初めてサルを用いた実験により証明したと発表した。
慢性腎不全に対する根本的な治療法はなく、腎臓機能を回復させる再生医療に大きな期待が掛かっている。東京慈恵会医科大学は、2019年より日本医療研究開発機構(AMED)の再生医療実用化研究事業の採択を受けて、大日本住友製薬とヒト iPS 細胞を用いた「胎生臓器補完法」による腎臓再生医療の実現を目標として、サルをレシピエントに共同研究を進めてきた。
明治大学およびバイオスも研究推進に協力している「胎生臓器補完法」は、ブタ胎児の臓器を使用するため、昨今の遺伝子改変技術の進歩により遺伝子改変ブタの臓器のヒトへの移植で注目を集めている「異種移植」技術も利用している。
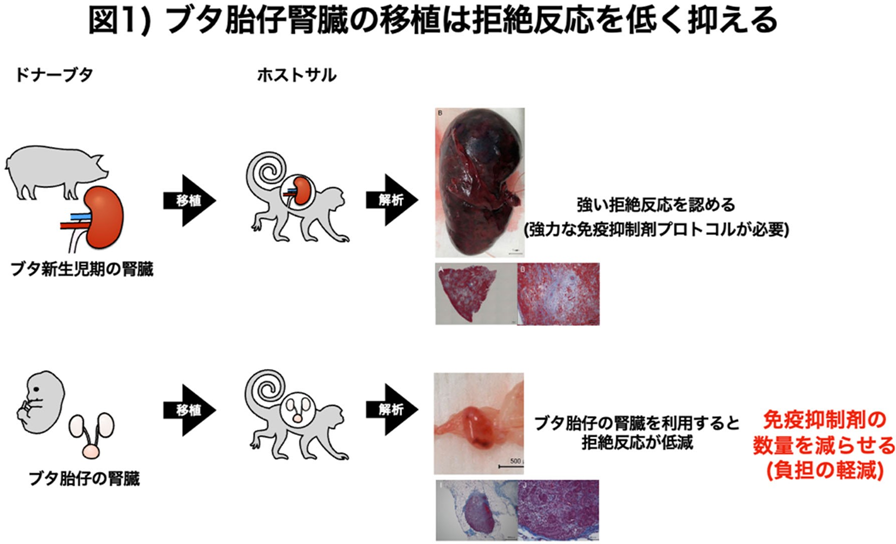
今回、ブタ腎臓のサルへの異種移植において、血管付きの異種移植法より、胎仔腎臓を移植して育てる異種再生法の方が、拒絶反応が弱いことを世界で初めてサルを用いて証明した(図 1)。同成果は、国際誌 Engineering で 2 月 23 日オンライン版で公開された。
腎不全をはじめとする臓器不全の根本的対策として移植医療が進められ移植患者の劇的な改善が見込めるようになった。だが、世界においても慢性的なドナー不足により一般的な治療法となっていないのが現状だ。
この危機的状況の打開策として、以前からブタを利用した異種移植が注目されていたが、多くの免疫抑制剤管理を行ったとしても長期の維持は難しく利用可能な技術には至っていなかった。
一方、完全にヒト iPS細胞から臓器を再生させる完全型の再生医療も生体で機能をもった実質臓器レベルのものはまだ出来ていない。
横尾氏らの研究グループは、世界でも独自な完全型再生医療と異種移植との利点を兼ね備えたキメラ臓器による「胎生臓器補完法」の研究を進めてきた。
研究グループは、これまで遺伝子改変したマウス胎仔腎臓にラットの腎臓の前駆細胞注入した複合腎臓(クロアカ:膀胱付き腎原基)をラットに移植することで再生するキメラ腎臓を作り得ることを証明してきた(山中, Nature Communications 2017)。
これを受けて実際の臨床に応用すべく、大日本住友製薬とブタの胎仔腎臓をベースにサルに移植する前臨床研究をスタートさせた(2019年)。小動物モデルによるメカニズム研究に合わせ、サル等のヒトに近い実験動物での立証を行い、膀胱付き腎原基移植技術の開発を目指したもの。
また、その基盤となるアカデミアの成果を実臨床にあげるためには産学連携が必要なところから東京慈恵会医科大学では産学連携講座 腎臓再生医学講座(バイオス社:林明男代表)を設置し、実験医学の世界的権威の小林英司博士を特任教授として招聘して同プロジェクトを推進してきた。
これまで胎仔の組織は、「移植において拒絶反応が出にくい」とは言われていたが、実際にブタの胎仔腎臓をサルへ移植しても生着ができ、さらに出生後の腎臓よりも免疫原性が低いかは不明であった。
同研究では、遺伝子改変を行っていない野生型ブタの胎仔腎臓と生後間もない新生仔腎臓を、臨床でも使用される免疫抑制剤のみを投与したサルに移植した。
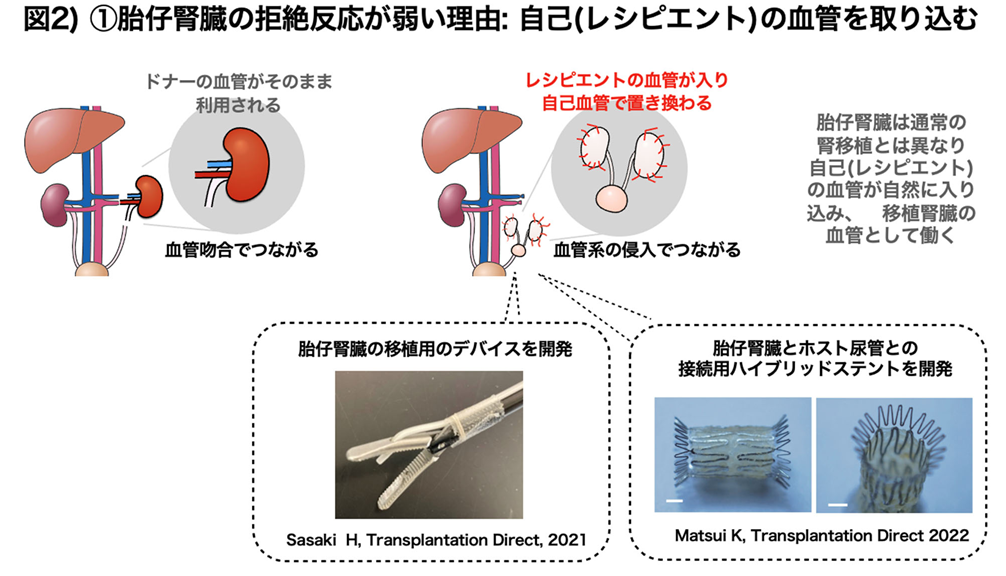
胎仔腎臓は、2つの腎臓と尿管膀胱を含む複合腎臓(クロアカ:膀胱付き腎原基)を顕微鏡下で採取して、サルの腹部大動脈と尿管に近い後腹膜下にポケットを作り、血管吻合を行わずにそのまま静置で移植した(図 2 右)。
一方、新生仔腎臓はサルの左側腎臓を摘出後、同所に血管や尿管ごと吻合し移植する方法を独自に開発し実施した(高村, Acta Cirurgica Brasileira 2021)(図 2 左)。
まず、現在米国FDAで臨床使用が承認されている免疫抑制剤を使用し、一匹のサルに 2 つの腎臓組織、すなわち、ブタ胎仔クロアカグラフトの静置移植と新生仔腎臓の血管吻合移植を行った。
その結果、ブタの新生仔腎臓は約2週間後に拒絶反応による組織傷害が強く見られ、移植腎臓を摘出することでサルの死亡を食い止めた。
一方、同時に移植されていた胎仔腎臓は、同一のサル体内で 2 カ月以上も大きな拒絶反応を起こすことなく糸球体や尿細管などが発育した。胎仔クロアカグラフトの免疫反応の弱さを再度検証するために臨床使用される免疫抑制剤を長期間使用しながらその生着を経時的に観察したが、移植されたブタの胎仔腎臓は徐々に発育を続けた。
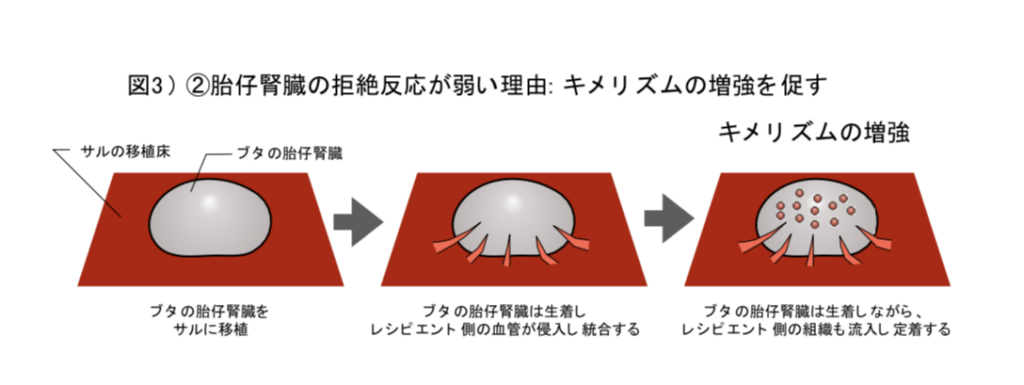
病理像ではレシピエントであるサルの血管が入り込んでおり(図 2)、さらにレシピエントの組織と一部キメラ化することも確認され(図 3)、胎仔腎臓移植の免疫拒絶の低減が実証された。
同研究結果は、ブタ胎仔の腎臓原器移植は霊長類での拒絶反応が現在臨床使用される免疫抑制剤でコントロールできることを示したものだ。
これまで異種移植は、移植されるドナーブタの多重遺伝子改変で進められてきたが、従来の異種移植とは異なる方法によるサルでの前臨床試験を成功させた意義は大きいと考えられる。
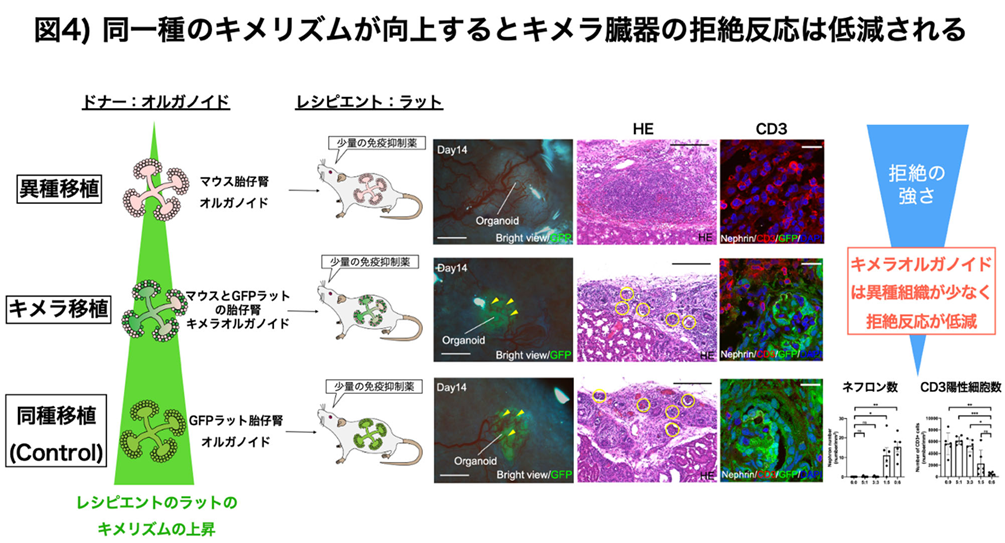
研究グループは、マウス―ラット間の小動物間の実験ではあるが、レシピエント(ラット)と同じ動物種の腎臓の構成成分(キメリズム)を高めたラットとマウスによるキメラ腎オルガノイド移植は、マウス単独の腎オルガノイドによる異種移植と比較しCD3陽性炎症細胞の浸潤とそれに伴う糸球体廃絶も軽度であり、キメラが異種の免疫拒絶反応を著明に低減できることを実験的に証明した(齋藤, Frontiers in Immunology 2022)(図 4)。
さらに、研究グループは、柔らかいブタ胎仔腎臓原器を腹腔鏡で安全に移植できるデバイス開発(佐々木Transplantation Direct 2021)(図 2 左下)や、移植し発育した膀胱とホストの尿管をつなぐハイブリッドステント(松井 Transplantatoin Direct 2022)(図 2 右下)の開発に成功しており、ヒト臨床で行うための準備を進めている。
今回、遺伝子改変をしていない通常のブタの胎仔腎臓をサルに「異種移植」できることを示したが、依然として多くの免疫抑制剤の投与が必要であった。
研究グループ独自の完全型再生医療と異種移植との利点を兼ね備えたキメラ臓器による「胎生臓器補完法」は、ブタ胎仔腎臓が患者の体内で育ちながら患者本人の腎前駆細胞がブタ胎仔腎臓の組織を置き換えることで免疫抑制剤の投与不要を目指している。
患者本人の腎前駆細胞を利用するための課題は、患者由来のiPS細胞から迅速に腎前駆細胞を作る技術であり、ブタ胎児腎臓の後者組織を置き換えるための課題は、薬剤によるブタ組織が消失する遺伝子改変ブタの作製である。研究グループでは、いずれの課題にもすでに共同研究を遂行中である。


