今後の脳内GBM治療・再発抑止への応用に期待
ナノ医療イノベーションセンター(iCONM、センター長:片岡一則氏)は11日、免疫チェックポイント阻害剤アベルマブにブドウ糖残基を持つポリマーを修飾した抗体を開発し、マウス脳内への効率的な送達や、悪性神経膠腫(GBM:グリオブラストーマ)の同所移植マウスで高い有効性と再発抑制効果を確認したと発表した。
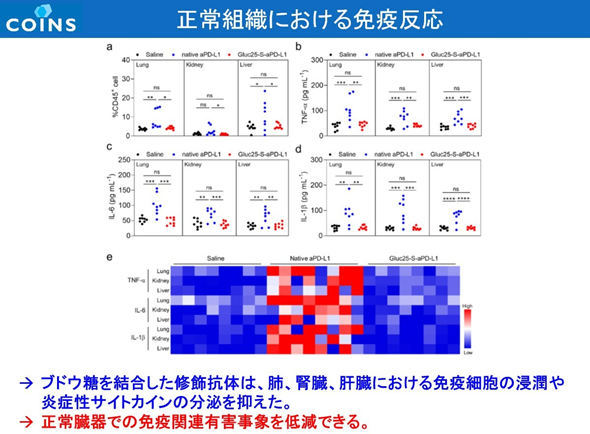
同研究成果は、東京大学大学院工学系研究科バイオエンジニアリング専攻との共同研究によるもので、Nature Biomedical Engineering に掲載された。Natureでは、ベルマブにグルコースを末端に持つポリマーを修飾することで、正常細胞への同剤の作用を回避し、「炎症性サイトカインの過剰産生」の問題を解決できる可能性を示したことが、最も評価される点となった。
加えて、悪性神経膠腫の同所移植マウスにおいて、アベルマブの腫瘍組織への集積性を未修飾のアベルマブと比較して33倍高値を示し、アベルマブの標準使用量の15%量を1回投与するだけで60%の完全奏効率を示したことから、今後、脳内GBMの治療・再発抑止への応用が期待される。
免疫チェックポイントは、免疫細胞であるTリンパ球(T 細胞)の活性を制御する分子機構である。がんにおいては、がん細胞の表面にあるPD-L1リガンドと呼ばれるタンパク質(PD-L1)と T 細胞の表面にある PD-1 受容体が免疫チェックポイントとして働き、これらが結合するとT 細胞のがん細胞への攻撃性が損なわれる。
この発見により、2018 年、京都大学・本庶 佑教授がノーベル賞(医学生理学賞)を受賞し、現在、6 種類の免疫チェックポイント阻害剤が、がん治療の臨床現場で使用されている。
だが、免疫チェックポイント阻害剤は、様々ながんに対して優れた有効性を示す一方で、悪性脳腫瘍(脳転移がんも含む)に対しては臨床試験で満足のいく有効性が示されていない。
その理由は、脳腫瘍の血管壁が形成する血液脳腫瘍関門によって、脳腫瘍への免疫チェックポイント阻害剤の集積が抑えられていることが一つの要因となっている。
一方、脳腫瘍内の免疫チェックポイント阻害剤濃度を治療可能域まで高めるために投与量を上げれば、免疫関連有害事象が生じてしまう。
そこで、同研究は、免疫チェックポイント阻害剤の脳腫瘍集積性を劇的に高める技術を開発し、治療の有効性と安全性の両立を目的に実施された。免疫チェックポイント阻害剤は、ヒトおよび動物の両方で免疫活性作用が確認されているアベルマブが用いた。
研究では、脳腫瘍においては、ブドウ糖をエネルギー源として利用するための代謝系が活性化していて、脳腫瘍へのブドウ糖の取り込みが亢進していることに着目。
免疫チェックポイント阻害剤にブドウ糖残基をもつ高分子を複数修飾して、免疫チェックポイント阻害剤を脳腫瘍に対して効果的に(4時間後に未修飾抗 PD-L1抗体の18倍)送達することに成功した。
脳腫瘍への集積量は、正常な脳組織の33倍あり、高い脳腫瘍選択性を示した。また、免疫チェックポイント阻害剤と高分子の間の結合を脳腫瘍内特有の環境下(還元的環境下)で切断されるように設計しているため、正常組織では高分子の結合により免疫チェックポイント阻害剤の活性を抑えながらも、脳腫瘍内では高分子が外れて免疫チェックポイント阻害剤が遊離して活性化する高分子化合物(Glc-ICI)を得ることができた。
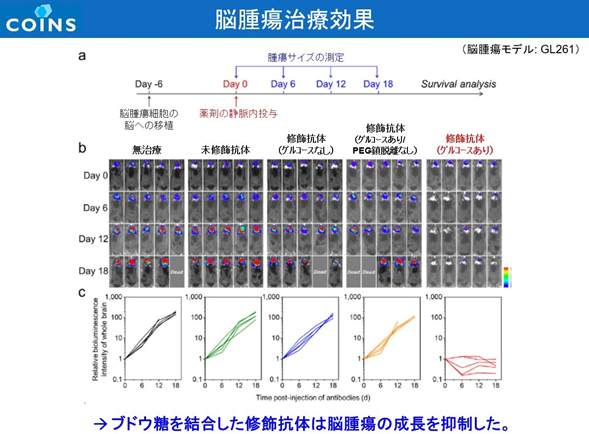
その結果、臨床の場で 免疫チェックポイント阻害剤の課題となる炎症性サイトカインの産生による免疫関連有害事象を抑えながら脳腫瘍内で強い抗腫瘍免疫を誘導することに成功し、マウスの同所GBMモデルにおいて60%の完全奏効率を得た。
しかも、投与回数は 1 回で、低用量で十分な効果が認められた。具体的には、標準的に用いられる薬剤量は10mg/kg 複数回投与であるのに対し、同研究では1.5mg/kgで1回投与の低用量で十分な効果が認められた。
Glc-ICIで処置したマウス脳腫瘍内の抗腫瘍免疫細胞を調べると、腫瘍に対する攻撃性を示すCD8+ T 細胞やナチュラルキラー(NK)細胞の浸潤数が増加し、免疫抑制を担う制御性T細胞(Treg)および骨髄由来免疫抑制細胞(MDSC)が減少するとともに、脳腫瘍内のマクロファージの極性も免疫活性性のM1タイプが免疫抑制性のM2タイプより優勢となっており、総じて脳腫瘍内の免疫状態が抗腫瘍状態に移行したことが確認できた。
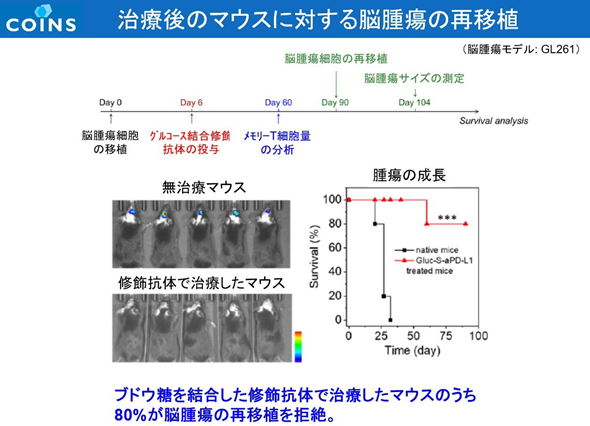
また、Glc-ICIで奏効し 60 日以内に腫瘍が消失(完全奏効)したマウスの脾臓には、エフェクターメモリーT 細胞が確認でき、そのマウスに GBM 細胞を再移植しても発がんが確認さなかった。
つまり、同法により GBMに対する免疫が長期間にわたって形成されることが確認できた。GBMは、再発頻度の高い悪性腫瘍であるが、この結果から GBMの再発抑止への応用が期待できる。