アストラゼネカは17日、第3世代不可逆的 EGFR 阻害剤「タグリッソ」について、P3相ADAURA試験において顕著な有効性を示したため、独立データモニタリング委員会(IDMC)の勧告に従って早期に非盲検化すると発表した。
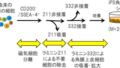
ADAURA試験は、完全腫瘍切除したIB期、Ⅱ期、ⅢA期の上皮成長因子受容体遺伝子変異陽性(EGFRm)非小細胞肺がん(NSCLC)患者を対象に術後補助療法としてのタグリッソの評価を行うP3試験。
ADAURA試験の主要評価項目は無病生存期間で、銅試験では、タグリッソをプラセボと比較し、最長3年の治療期間で評価した。同試験は引き続き、副次評価項目である全生存期間の評価を行う。なお、IDMCからは、同試験における新たな安全上の問題は提起されなかった。同試験の詳細データは、今後の学会で発表される予定である。
タグリッソは、第3世代不可逆的 EGFR 阻害剤であり、EGFR 感受性変異および EGFR T790M 耐性変異の両方を阻害するよう設計されており、中枢神経系転移に対する臨床活性も有している。
現在、タグリッソ40mg 錠および 80mg錠の1日1 回経口投与は、EGFR 遺伝子変異陽性進行NSCLCの 1 次治療として米国、日本、中国および EUを含む 80 か国で承認されており、EGFR T790M 変異陽性進行 NSCLCの2次治療としても米国、EU、日本、中国、EU を含む87カ国で承認されている。
また、タグリッソは術後補助療法(ADAURA 試験)、切除不能な局所進行例(LAURA 試験)、転移がんにおける化学療法との併用療法(FLAURA2 試験)、ならびに EGFR 阻害剤に対する耐性に取り組むため
他の新薬候補との併用療法(SAVANNAH 試験、ORCHARD 試験)においても検討が進んでいる。
なお、EGFR遺伝子変異陽性非小細胞肺がんの術後補助療法に対するタグリッソの適応は、本邦では未承認である。
タイトルとURLをコピーしました