
新型コロナウイルス感染症に対する治療薬は、現時点では特異的なものはない。特例承認を受けているレムデシビル(エボラ治療薬、RNA合成阻害剤)は、人工心肺装置(エクモ)が必要になる前に有効で、中等度から重症への移行を防止するほか、入院期間を短くする特徴もある。ただし、エクモを使用している患者には効果がなく、人工呼吸器に繋ぐ前の治療薬である。
承認申請中のアビガン(抗インフルエンザ薬)は、症状のないもっと軽症の患者に使用する。
11月21日にFDAが、緊急使用許可(EUA)を与えたリジェネロンの新型コロナウイルス感染症(COVID19)の抗体カクテル療法は、初期症状を示す患者が対象である。10月に米国のトランプ大統領が新型コロナに感染した際に受けた同療法は、新型コロナに罹患して治癒したヒトの中和抗体を模造した人工抗体を投与するというものだ。どの抗体が最も効くかを試す余裕がないため、効果がありそうな2種類のモノクローナル抗体を組み合わせている。

来年には新型コロナ用実験動物モデルが確立し新薬登場も
他の治療薬は、現時点ではあまり明るくない。その理由は、創薬において適切な動物実験モデルが確立されていないためだ。新型コロナウイルス(SARS-Cov-2)は、もともとコウモリのウイルスと言われており、ネズミには罹らない。小動物の中で唯一感染するハムスターも、下痢の症状しか出ない。しかも、自然に治癒してしまうので、ヒトの症状とは全く合わない。フェネックやネコも、罹患するが症状は出ない。
肺炎治療や発熱を防止するための動物実験モデルがないため、通常、創薬で行う大量に候補化合物を作って、スクリーニングをかけて小動物に投与し、さらに大型動物に投与する手法が取れない。現在、治療薬の効果が出現しない大きな要因は、動物実験モデルが無いためである。
今、阪大などでトランスジェニックも含めた実験動物モデルの作製を進めている。おそらく来年には、いくつかの実験動物モデルができて、治療薬候補も出現するだろう。
だが、今のところは、治癒したヒトの抗体から治療薬を作る手法以外に手立てはない。このタイプの治療薬は、イーライリリーを始め数社が手掛けており、同タイプの薬剤が何種類か誕生しそうだ。緊急使用許可と特例承認は異なるが、治療薬もいくつか目途が着いてきたと思われる。
新型コロナ治療は悪化パターンの判明により死亡者減少
新型コロナ感染症の治療においては、症状が悪化するパターンが判ってきたので、該当する人に早めの人工呼吸器を使うとか、抗血栓剤を先に投与しておくなどの手法が取られている。それに伴い、死亡者数も減少している。
とはいえ、基本的に、新型コロナ感染症治療は、自然経過で良くなっていくのを待つしかない。そのためには時間が掛かるので、感染を予防するワクチン開発が非常に重要になる。
中和抗体作成とと細胞性免疫の両機能を持つワクチンが理想
ワクチンは、免疫を利用して創製するが、現在、免疫を向上させる健康食品も売れている。コロナ禍では不景気が一般的であるが、「自分の体は自分で自衛する」という観点から健康食品の通販は意外に好調である。
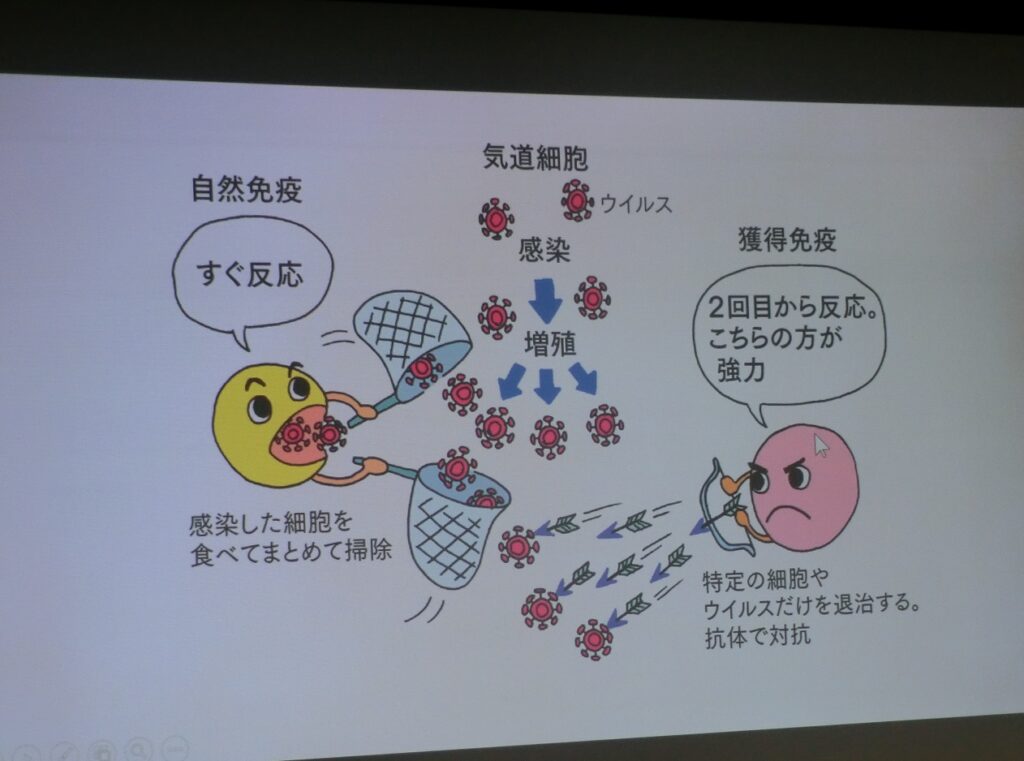
健康食品による免疫療法は、自然免疫によるものだ。自然免疫は、感染した細胞や病原体をすぐに貪食して掃除する機能である。
これに対して、ワクチンは獲得免疫によって機能を発揮する。獲得免疫は、特定の細胞やウイルスだけを発見して、中和抗体を作って攻撃する。今回、新型コロナウイルスは、獲得免疫を得ることができないためなかなか感染が防げない。
例えて言えば、自然免疫は強すぎると自己免疫疾患になるので警察のような役割をしている。一方の獲得免疫は、自衛隊のようにより強力なもので、2つの免疫カテゴリーでバランスを取っている。今回は、獲得免疫を得るためのワクチンを作っていく必要ある。
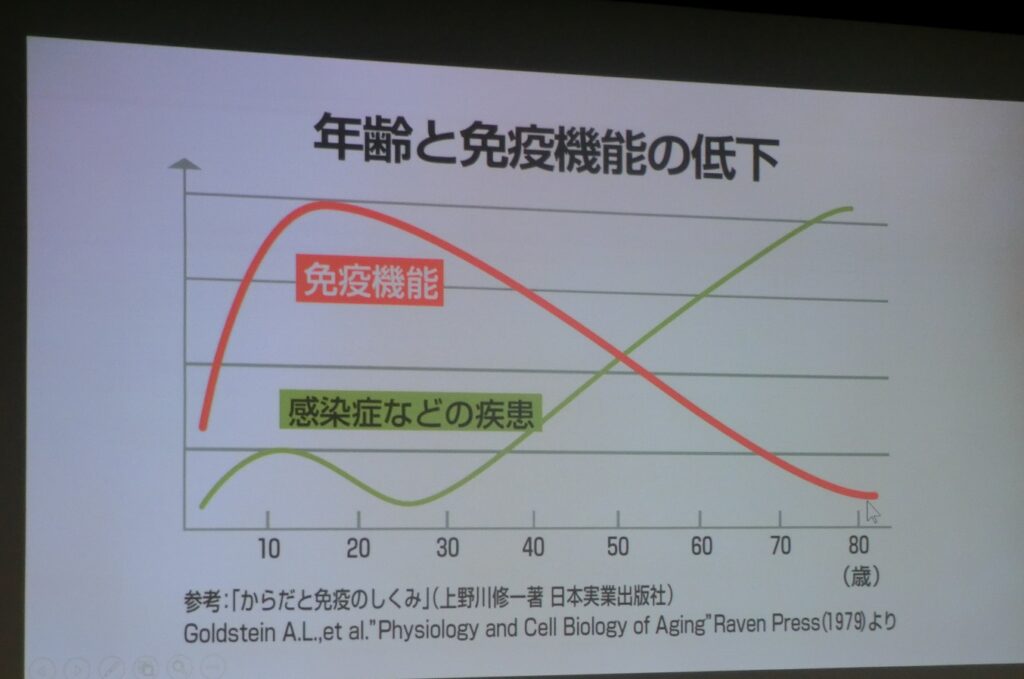
免疫機能は、18~20歳をピークに下降していき、免疫老化に伴って感染症が増加していく。自然免疫は、樹状細胞、NK細胞、好中球がその役割を示す。獲得免疫は、樹状細胞からの指によりヘルパーT細胞で中和抗体を作ってウイルスを攻撃する。その一方でキラーT細胞は、ウイルスが増えている細胞を殺していく。獲得免疫は、体内でウイルスが増える場所を攻撃していくため、重症化への予防にもつながる。基本的にワクチンは、中和抗体を作る機能とウイルスの増えている細胞を殺す「細胞性免疫」の二つの機能を有しているものが望ましい。
各種新型コロナワクチンのメリット・デメリットの理解が重要
今、ワクチンの開発で先行しているのは、英アストラゼネカ(タイプ:ウイルスベクター)、米ファイザー(同RNA)、米モデルナ(RNA)で、これらは全て遺伝子治療の技術を活用している。
遺伝子治療は、これまで疾患を有する患者さんの治療でさえも使用許可を得るのに1~2年を要し、がんでもなかなか使用許可が降りなかった。今回、ワクチンとしてここまで多くの人に使われるのは想定外であった。
また、アストラゼネカのワクチンには、アデノウイルスベクターが使われている。そのアデノウイルスが含まれたワクチンを健常人7億人に同時に投与するのは、30年以上遺伝子治療に従事してきた我々にとっては、驚きと隔世の感があり、安全面をしっかりと見定める必要があると考える。
過去の例では、アデノウイルスで死亡例が出たこともある。肝機能障害の副作用について、特に、ハイリスクの人にワクチンを打つ場合はかなり初期のところでしっかりとフォローしなければならない。
これらのワクチンは、遺伝子治療の手法が全て異なるため、それぞれにメリット・デメリットがあり、それをきちんと理解して使う必要がある。これまでのインフルエンザワクチンのように、全て同じものを打っていたのとはかなり異なる。
この辺りを国民にしっかりと理解してもらわなければ、何か問題が起こった時に子宮頚癌ワクチンのように一斉に拒否反応が起こる可能性もある。その一方で、「ワクチンは打っても必ず大丈夫である」という安全神話的なものがあっても困る。使用者のリテラシーをかなり上げることをしなければ、なかなか普及しないと思われる。
ワクチンは、「ウイルスワクチン」、「ウイルスベクターワクチン」、「タンパク質ベースのワクチン」、「核酸ワクチン」の4つに分類される。ウイルスワクチンは、従来のタイプのワクチンで、インフルエンザや麻疹、ポリオと同様にウイルスそのものを不活性化・弱毒化したものである。
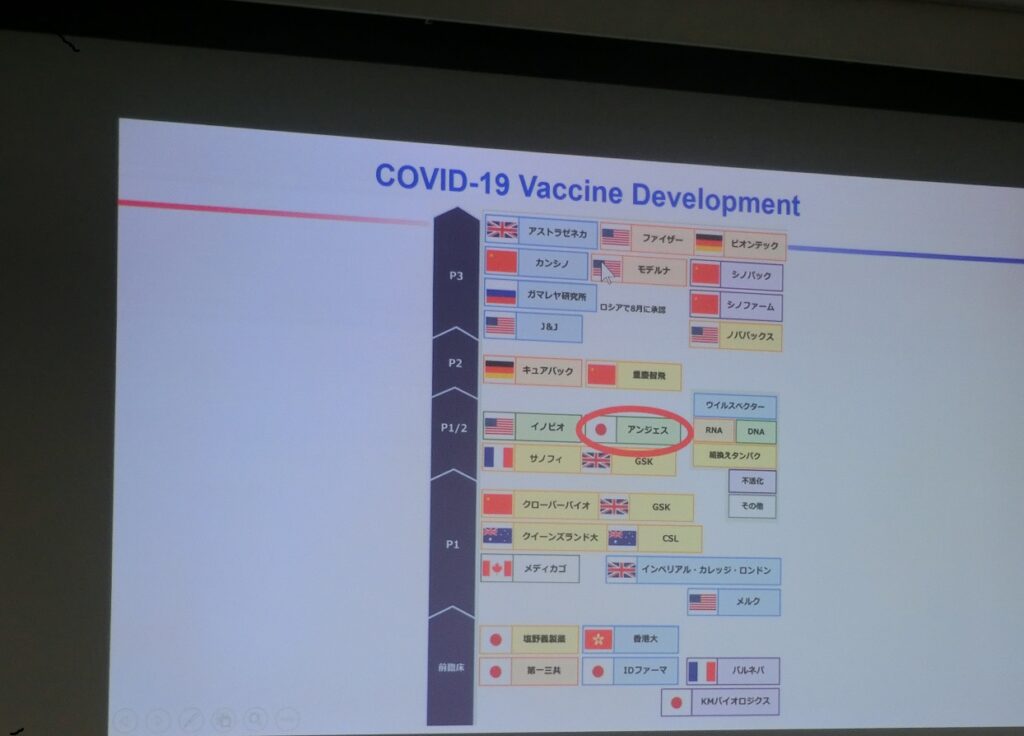
今、最も進んでいるのが、遺伝子治療を応用したウイルスベクターワクチンである。アデノウイルスの中にスパイク蛋白の遺伝子を組み込んで、注射して体内でスパイク蛋白を作る手法で、現在、オックスフォード大学とアストラゼネカが開発している。
ウイルスの一部のスパイクの蛋白を組み替え型にするのが「タンパク質ベースのワクチン」である。
核酸ワクチンには、DNAワクチンとRNAワクチンがある。RNAワクチンは、DNAから作ってRNAの段階で投与する。
基本的に有効性の高いワクチンは、アデノウイルスを使ったウイルスベクターワクチンで、抗体の発現が非常に多い。ただし、副作用も最も多いと想定される。続いて、RNAワクチンも有効性が高いが、こちらも副作用がかなり出ている。
一方、DNAワクチンは非常に安全性が高いが、抗体の発現効率が悪いので、ウイルスベクターワクチン、RNAワクチンに比べると有効性は下がる。
従来のウイルスワクチンも、基本的に有効性はあまり高くはない。麻疹では非常に高いものの、インフルエンザでは40~50%程度で、総じて安全性の高いものは有効性が低い傾向にある。
ワクチン開発は欧米は有用性、日本は安全性を重視
ワクチンは、欧米と日本との考え方の違いが浮き立っている。欧米は有効性の高さに着目しており、副作用が出ても重篤でなければ甘受できる範囲にある。従って、「できるだけ有効性の高いワクチンから進めて行こう」という考え方がその根底にある。
一方、日本では、我々のアンジェスも含めてどの企業も、「過去にある程度安全性が高いと思われるものからスタートして、安全性を担保しながら有効性を少しでも上げて行く」という考えのもとに開発を進めている。
日本の考え方から言えば、ファイザーやモデルナの有効率95%の数字は非常に高いものの、副作用の点では厳しいと思われる。
現在、アンジェスのDNAワクチンの有効性は50~70%程度であるが、「有効性と安全性を考慮してどちらのワクチンが良いか」ではなく、「どちらが日本人の好みに合うか」というところに行き着くだろう。いずれにしろ、未曾有のワクチン開発競争をしているため、色々な意味で選択肢は非常に難しい。
アンジェスのDNAワクチンは既存の遺伝子治療薬がベースで高い安全性
アンジェスのDNAワクチンは、プラスミドDNAの中に新型コロナウイルスのスパイクの遺伝子を入れ、それを筋肉注射して体内でスパイクを作り、スパイクに対する抗体を出現させる。
新型コロナウイルスが体内に入っても、この中和抗体が働いて感染を防止する、あるいはウイルスの増加を防いで重症化を防止することが期待される。
プラスミドDNAワクチンは、WHOのワクチンガイドラインの中で、「抗原特異的なB細胞刺激による抗体産生と、ウイルスが増殖している細胞を殺す細胞性免疫の理想的なメカニズムを有する」と記載されている。加えて、「ベクターに対する抗体はなく、繰り返し投与が可能」、「製造が容易で製剤の安全性に優れている(製造期間が6~8週間と短い、抗原ウイルスを扱う必要がない、生産は精製施設で可能、長期備蓄可能、特別な設備・施設が要らない)」などの特徴も列挙されている。
ワクチンの繰り返し投与については、アストラゼネカのアデノウイルスワクチンは、アデノウイルスに対する抗体ができるので、1年後にもう1回投与しようとしても効果がなく、一度打つとそれで終了になる。2回目、3回目以降もワクチンを打つ必要があれば、別のタイプのワクチンを選択しなければならない。
ロシアや中国のワクチンも同様で、現在開発されているワクチンの約半数がウイルスベクターを用いたものである。従って、アストラゼネカのワクチンが世界中で幅広く投与されてから、新たなパンデミックが起これば、今回新型コロナワクチン開発に参加してきたベンチャーの約半数が参加できなくなる。
次のパンデミックを考えれば、プラスミドDNAワクチンの「繰り返し投与可能」という特徴は、大きなポイントとなる。ちなみに、RNAワクチンも繰り返し投与が可能である。
アンジェスのプラスミドDNAワクチンは、既に血管再生遺伝子治療薬として承認されている「コラテジェン」がベースになっているため、安全性は非常に高い。
世界初のプラスミド(DNA分子)製品であるコラテジェンは、HDF遺伝子を発現する血管再生治療薬のため、車に例えればレクサスのようなものだ。一方、今回のプラスミドDNAワクチンは、何の薬効もなく、新型コロナウイルス表面に発現するスパイクタンパク質作成のみを目的とするため、カローラくらいのイメージになる。
このようにプラセミドDNAには、より高いところで安全性・品質が確認されたデータがあったことが、アンジェスのワクチンが早く臨床入りができた大きな理由の一つでもある。
よく「DNAワクチンは承認された前例がない」と言われる。確かにDNAワクチンとしては承認されていないが、プラスミドを使ったコラテジェンが実用化されているため、適切な保管方法や製造方法は他のワクチンよりも優位ではないかと考えている。DNAプラセミドの商業化に伴う保管品質については、厚労省が許可している。
新型コロナDNAワクチンは、投与方法とメカニズムもコラテジェンと同様である。冠状のDNAが注射で投与されて筋肉に入るとRNAを作成するので、コラテジェンで得た安全性データがフルに活用できる。
ちなみに、このRNA段階のものをたくさん作って打つのがRNAワクチンで、メカニズム的には同じだが、使うモダリティが異なる。RNAは、DNAからRNAに変わる必要がないため、たくさん抗原が発現できるメリットはある。
アンジェスのDNAワクチンP2/3入りで先行グループに追いつく
アンジェスのDNAワクチンの臨床試験進捗状況は、本年6月より大阪市大病院で、健康成人を対象とした、1mg2週間隔2回筋肉内接種(15例)、2mg2週間隔2回筋肉内接種(15例)のP1/2試験を実施した。
9月からは、大阪大学病院で、健康成人を対象とした、2mg2週間隔2回筋肉内接種(10例)、2mg4週間隔2回筋肉内接種(10例)、2mg2週間隔3回筋肉内接種(10例)のP1/2試験を実施し、投与方法を変えたり投与回数を増やしてより有効性が上がる手法を同定している。
これらの試験結果から安全性に関して特に大きな問題はなかったため、12月より健康成人を対象としたプラセボ比較P2/3試験が、関西および関東エリアの8 施設で開始された。同試験は、500症例の被験者への接種を行い、ワクチンの用法および用量における安全性と抗体価測定によるワクチンの有効性の評価を目的とするもので、2mg2週間間隔2回筋肉内接種(250例)と、2mg4週間間隔2回筋肉内接種(250例)を実施する。それぞれに、プラセボ50例が含まれている。

臨床試験では、プラスミドDNAワクチンを投与する前にPCR検査と抗体検査を行って、過去に感染が無いかきちんと調べるようにしている。その理由は、プラスミドDNAワクチンの効果を確実に見るためと、ADE現象を少しでも減らすためである。検査には、PCR検査、抗体検査があり、検査の時期とメリットが異なる。こういった検査をうまく組み合わせて新型コロナウイルスの流行を把握することも非常に重要である。様々な検査法を駆使して、新型コロナウイルスの病態を解析研究をして、できるだけ被験者の安全を保ちながらワクチン開発を行うことを今進めている。

現在、最も先行している新型コロナワクチンは、米国ファイザー、米国モデルナ、独バイオ企業ビオンテック、英国アストラゼネカ、中国のカンシノ、ロシアのガマレヤなどで、いずれもP3段階にある。アンジェスのDNAワクチンもP2/3がスタートし、やっと先行グループに追いついた。
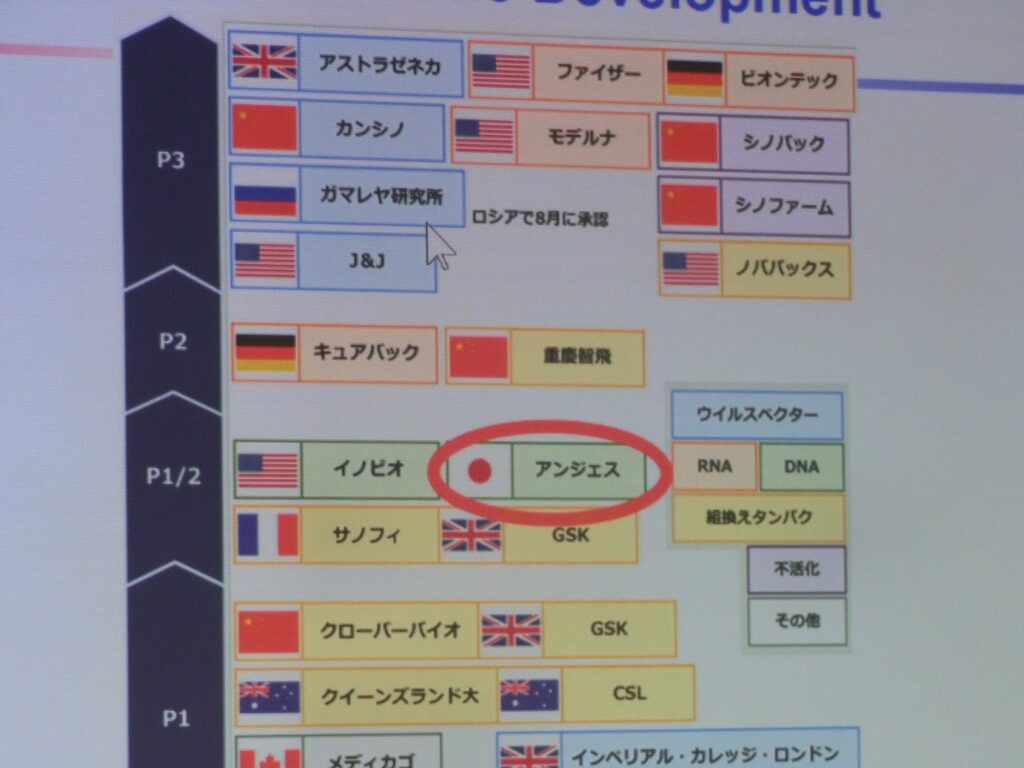
アンジェス
安全・安心をキープし着実に有効性向上して早期実用化を
とはいえ、ファイザー、モデルナの治験結果発表では90%以上の有効性が報告されており、他の先行ワクチンも良い成績が示されている。ここまでの有効性が出るとは思わなかったので、追いかける側からすると「非常に大変な思い」がある。我々は、基本的な発想として、「安全・安心のところをキープしながら有効性を着実に上げていく」という方法で臨むしかない。
第一世代、第二世代、第三世代と様々なモダリティ(創薬手法)を組み合わせて、70%程度の有効性を目指して開発を進めて行こうと考えている。
また、先行グループは、数万人規模の治験を行っているため、そこに至るように準備を整えてさらに大規模な治験を企画している。
今回モデルナの治験の新型コロナ感染率をみると3万人で約100人程度であるが、日本の感染率は20万~30万人で100人程度であるため、日本国内で大規模治験を行うのは難しいので、海外での治験実施を視野に入れている。
製造に関しては、プラスミドは大腸菌の中で増やすため、ビール工場のような大きなタンクがあれば簡単に大量生産可能だ。RNAワクチンの大量生産は難しく、大量生産の容易さはDNAワクチンの大きなメリットになっている。
500ℓのタンクでは25万人分の製造が可能だが、5000ℓの製造タンクを作れば250万人分製造できる。それが4基あれば1000万人分ということで、タンクさえあれば大量生産は難しくない。製造はタカラバイオが行うが、そこにAGC(旧称 旭硝子)やシオノギファーマも加わって、さらに製造能力の増大を図っている。
気になるDNAワクチン実用化の見通しについては、P2/3相試験のデータが出てくれば準備は整う。だが、今のところ厚生労働省のワクチンガイドラインで、どこまでのデータが必要かが明確にされていないので、今後当局と相談して、できるだけ早期の実用化を目指したい。


