加齢性筋減弱症など運動困難な患者に対する画期的な治療法確立に期待
東京都立大学大学院人間健康科学研究科の古市泰郎准教授らの研究グループは15日、培養筋芽細胞の移植による筋量増加に成功したとことを明らかにした。
筋の幹細胞の移植は、骨格筋組織が損傷しているような筋疾患に対しては有効性が確認されている一方で、加齢による筋萎縮のように筋線維がやせ細るだけで損傷していない場合には、細胞が生着しないという問題があった。
こうした中、古市氏らは細胞外基質(ECM)を用いる新しいアプローチでこの課題を克服した。培養した筋芽細胞を、ECMを含む液に浸してマウスに移植することで、筋線維の損傷がなくても細胞が生着し、筋量を増加させることに成功した。
さらに、移植細胞の数を増やすことで、コラーゲン沈着による線維化を抑えつつ、生着効率を高められることも確認した。これにより、骨格筋重量が約10%増加するという成果が得られた。
同研究は、損傷していない骨格筋に対する細胞移植の有効性を初めて示し、骨格筋再生医療の新たな道筋を切り拓くもの。今後は、ECMのいずれの因子が細胞の生着に関与するかを解明し、ヒトへの応用を目指した研究を進めていく。この技術は、加齢性筋減弱症や廃用性筋萎縮症など、運動が困難な患者に対する画期的な治療法となることが期待される。
同研究成果は2025年1月14日に国際科学誌 Frontiers in Cell and Developmental Biologyのオンライン版に掲載された。なお、同研究は、科学技術振興機構(JST) 創発的研究支援事業(JPMJFR205K)の支援のもと実施された。
加齢や運動不足による骨格筋の萎縮は、身体機能の低下や疾病への抵抗力の減少を引き起こし、生活の質を著しく損なう。特に、高齢者や筋萎縮が進行した方にとって、筋力トレーニングのような負荷の高い運動を行うことは現実的に難しい場合が多い。そのため、骨格筋の萎縮を予防・治療する革新的な方法の確立が求められている。
骨格筋再生医療は、筋幹細胞(筋肉を形成する未熟な細胞)を培養して筋組織に移植することで筋量を増加させるアプローチとして注目されている(図1)。 だが、これまでの研究では、筋ジストロフィー症など筋線維が損傷している場合には筋幹細胞の移植の有効性が示される一方で、加齢による筋萎縮のように筋線維が健全な場合(筋線維がやせ細っているのみ)では細胞が生着しないという問題があった。
さらに、筋幹細胞は高い生着能力を備えている一方、シャーレで培養すると筋芽細胞に分化し、組織への生着力を失うという課題があった。骨格筋は全身の約40%を占める大きな組織であるため、筋幹細胞ではなく筋芽細胞として大量に増殖させて移植させることが理想であるが、その解決策は長らく不明であった。
同研究では、これらの課題に対する新しい解決策として、細胞外基質(ECM)を活用する可能性を探った。
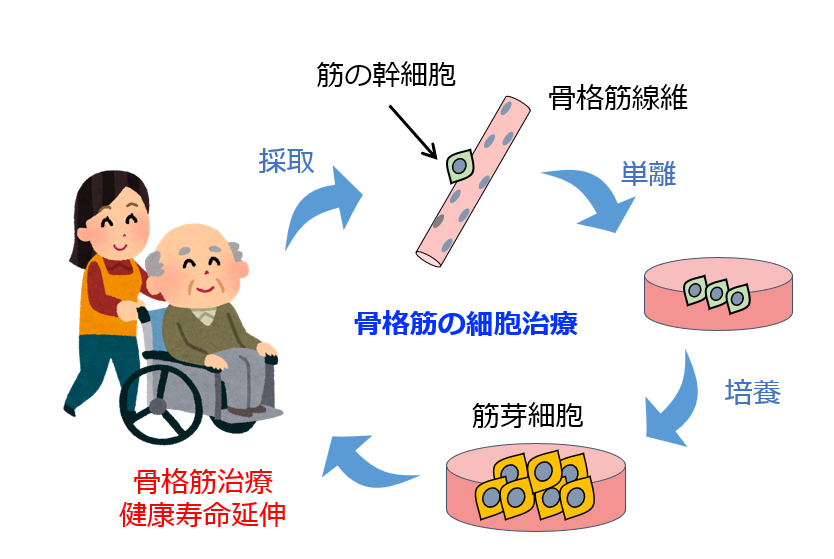
図1 骨格筋の再生医療
生体内の細胞は、その周囲を細胞外基質(ECM)とよばれる「足場」構造で囲められており、このECMは細胞の生存や機能に重要な役割を果たしている。一般的に、培養実験では筋芽細胞をシャーレで培養する際に、その表面をECMでコーティングすることで細胞の増殖や分化を可能にしている。同研究では、このECMを細胞移植に応用し、筋組織への細胞の生着を促進できるかを検証した。
まず、通常は生理食塩水に懸濁して移植する細胞に、ECM溶液をさらに加えて移植し、その生着量を評価した。
具体的には、緑色蛍光タンパク質(GFP)を発現するマウスから採取した筋芽細胞(ドナー細胞)を野生型マウス(GFPを持たない)の下肢筋に移植した。3週間後に筋組織内のGFP陽性細胞を定量したところ、筋線維を事前に損傷させる処理を行わなくても細胞が生着することを確認した(図2)。
一方で、筋組織を薬理的に損傷させた場合には、ECMの効果が減弱していた。
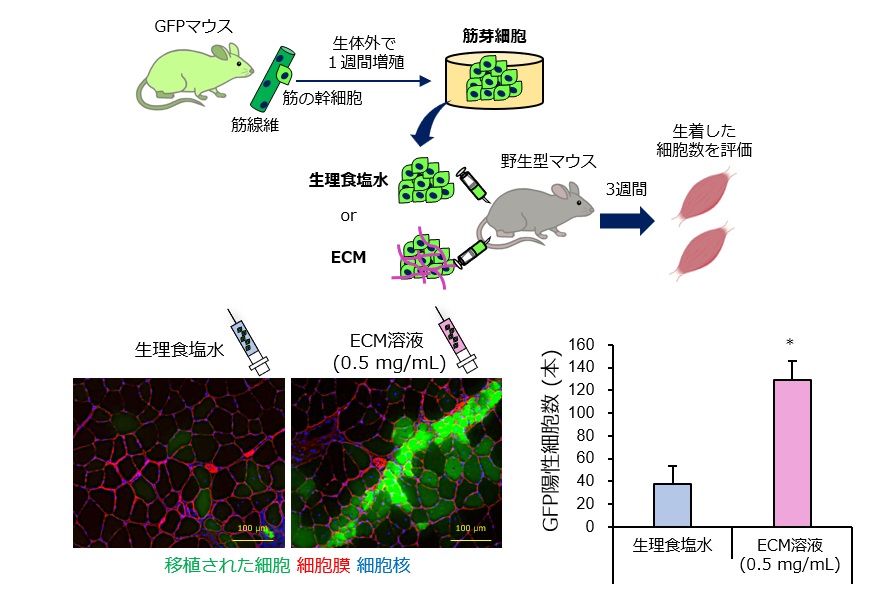
図2 ECM溶液は損傷していない骨格筋へ細胞を生着させる
GFPマウス由来の筋芽細胞を単離・培養し、生理食塩水またはECM溶液に懸濁して野生型マウスの骨格筋に移植した。3週間後に骨格筋を組織学的に解析した結果、ECM溶液を用いた移植群では、GFP陽性細胞(移植された細胞)の数が有意に多いことが確認された。
さらに、細胞外基質の濃度を調整することで生着率に与える影響を検討した。ECMの濃度を0.5mg/mLから5.0 mg/mLまで段階的に増加させたところ、2.5 mg/mLでGFP陽性細胞が最も高い生着量を示した。
だが、この条件下では筋線維間にコラーゲンなどECM由来のタンパク質が過剰に沈着し、線維化による筋機能への悪影響が懸念された。
そこで、移植する筋芽細胞の数を10倍に増やし、沈着の抑制を試みた。この手法では、生着細胞数がさらに増加し、コラーゲン沈着量も低減することが確認された。また、マウスの前脛骨筋(ぜんけいこつきん、重量約50 mg)に100万個(もとの10倍)の筋芽細胞を移植した場合、移植細胞が筋断面の約10%を占め(図3)、筋重量が約10%増加した(図4)。
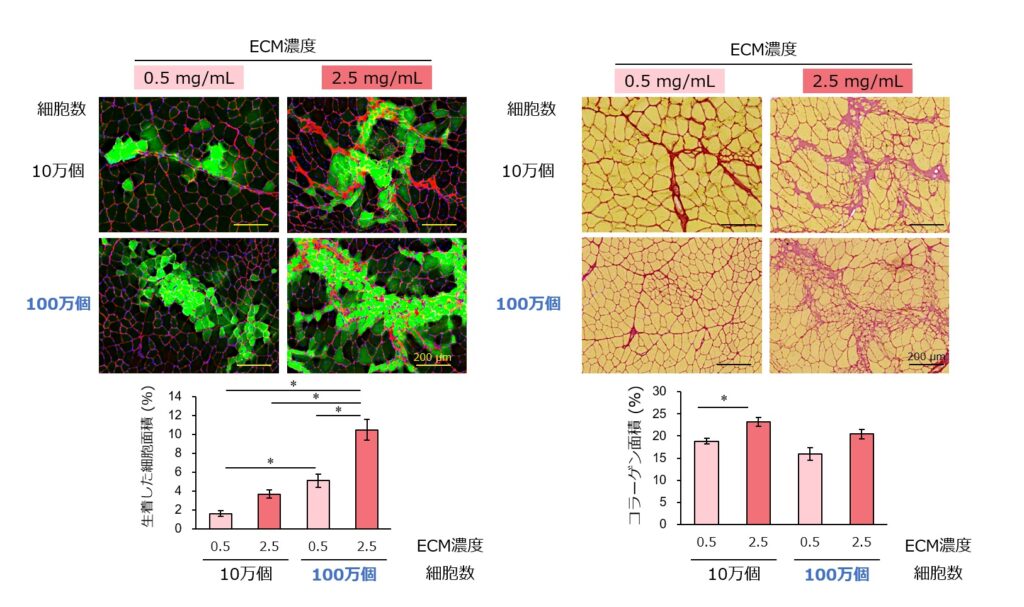
図3 移植する細胞数の増加はコラーゲンの沈着を抑制し、生着率を向上させる
ECM濃度を増加させるとコラーゲン沈着が増加する一方、移植する細胞数を増加させることで、コラーゲン沈着量は生着した細胞量に比して抑制されることが確認された。
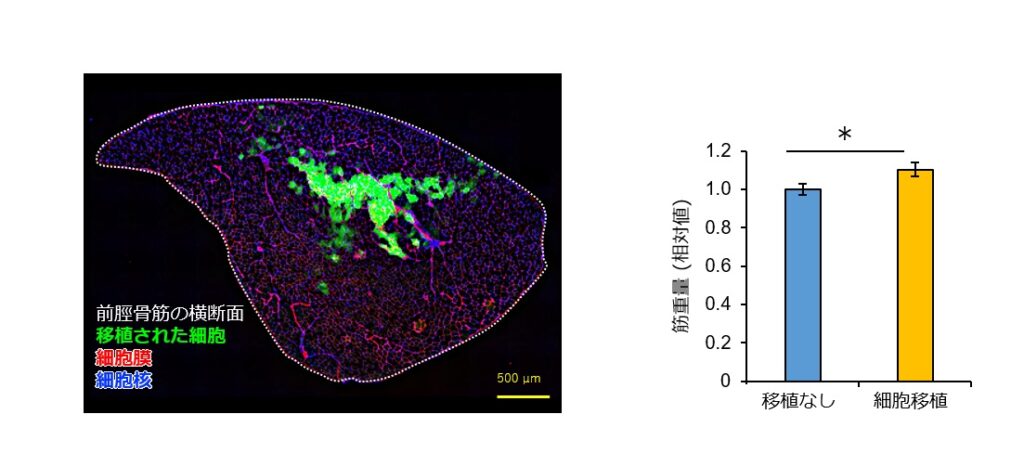
図4 筋全体の写真と細胞移植による筋重量の変化
ECMの濃度を2.5 mg/mL、細胞数を100万個に設定して移植した場合、筋組織全体の約10%の面積を移植細胞(GFP陽性細胞)が占めるまで生着した。前脛骨筋の重量は細胞移植によって有意に増加した。
同研究では、筋力への影響も検討したが、残念ながら筋力の有意な増加は観察されなかった。さらに詳細な解析を行ったところ、移植されたGFP陽性細胞の多くが未熟で小型の状態であることが判明した。このことから、細胞が筋線維として機能を発揮するまでには、これらを成熟させる必要性が示唆された。
だが、移植細胞の周囲には運動神経や毛細血管が形成されていることも観察され、これらが成長すれば筋力増強につながる可能性がある。
骨格筋の重量や筋力を増加させるには強度の高い運動が必要であるが、高齢者や疾患を持つ方にとっては困難な場合が多い。細胞移植は、迅速かつ効果的な筋萎縮治療法として期待される。同研究では、筋線維が損傷していない筋の萎縮においても、生体外で培養した細胞の移植で筋量を増加させられることを実証した。
この成果は、骨格筋再生医療に新たな道を拓くもので、細胞外基質のしくみをさらに解明することで、治療効果の向上が期待される。将来的には、この技術をヒトへ応用し、筋萎縮症や加齢性筋減弱症の治療に役立てることを目指す。


