〜シングルセル解析から見えてきた、ヒストンの調節による大規模な遺伝子活性化システムの存在〜
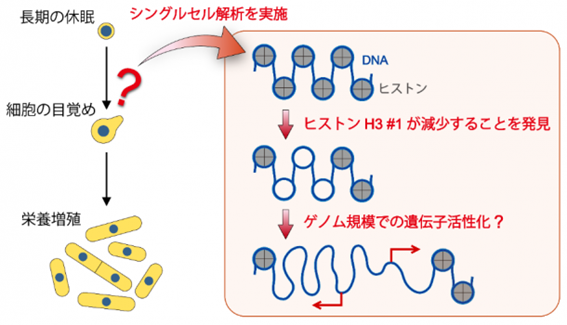
早稲田大学理工学術院の佐藤政充教授および同大大学院先進理工学研究科博士2年の露崎隼氏の研究グループは、シングルセル解析技術を改良することで、分裂酵母細胞が休眠から目覚める際の遺伝子の発現状態の変化について解明した。 同研究成果は、早稲田大理工学術院の竹山春子教授および細川正人次席研究員の研究グループ、産総研・早大 生体システムビッグデータ解析オープンイノベーションラボラトリ(CBBD-OIL)との共同研究によって得られたもの。
共同研究では、休眠打破に重要とみられる遺伝子を網羅的に見つけ出し、中でもヒストンH3遺伝子の変動が極めて重要な役割を果たすことを明らかにした。
そもそも、休眠と目覚めに関する謎はつきない。「細胞は休眠しているにも関わらず、周囲の環境に栄養が供給されたことを認識できるのはなぜか」、「それがどのようにヒストンH3 遺伝子の発現を変動させるのか」、「そもそも栄養がなくても死なずに生存を維持できる“休眠状態”とは細胞にとってどのような状態なのか」などが挙げられる。
植物の種子では、1000年前につくられた種子でさえも発芽できることが示されている。周囲に栄養がなくても休眠により長期にわたり生存を維持できる「省エネルギー」と「長寿」の秘訣が隣り合わせで胞子に隠されていると考察される。このことは、動物においては「がん化」という不都合な目覚めのメカニズム解明と予防策の究明に繋がる可能性が示唆される。
ヒストンH3遺伝子の制御による染色体のゲノム規模での変化は、受精卵からの発生、植物種子の発芽、がん細胞の増殖再開のメカニズムと類似している。従って、ヒストンを人為的に制御すれば、あらゆる生物で細胞の休眠打破を人工的にコントロールできると推測される。
今後、同研究は、様々な細胞が休眠から増殖を始めるメカニズムの解明に繋がり、新たな制がん標的遺伝子の特定や、がん細胞の増殖を抑える創薬への道筋になるものと期待される。同研究成果は、9日に「Nature Communications」のオンライン版に掲載された。