JCRファーマは2日、松島小貴東京慈恵医大遺伝子治療研究部助教、日置寛之順天堂大医学研究科脳回路形態学教授らとの共同研究で、脳への治療タンパク質輸送によるライソゾーム病(LSD)や神経変性疾患の新たな遺伝子治療法を開発したと発表した。
血液脳関門通過型の治療タンパク質を用いた遺伝性疾患のGM1ガングリオシドーシスモデルマウスに対するアデノ随伴ウイルス(AAV)ベクターによる遺伝子治療法を確立したもの。同システムは、。研究成果のポイントは次の通り。
・ 遺伝性疾患のGM1ガングリオシドーシスに対して有効な新たな遺伝子治療法を確立した。
・ 遺伝子治療用ベクターとして、J-Brain Cargo技術を応用した抗体融合酵素を発現するアデノ随伴ウイルス(AAV)ベクターを開発した。
・ GM1ガングリオシドーシスモデルマウスに対して治療を行い、生化学的・病理学的・行動学的に有
効性を実証した。
これらの研究成果は、本年4月8日にThe Journal of Clinical Investigation に掲載された。
GM1ガングリオシドーシス (GM1)は、ライソゾーム病 の一つで、ライソゾーム酵素であるβガラクトシダーゼ (βgal)をコードするGLB1遺伝子の遺伝子変異で発症する遺伝性疾患である。
βgalの欠損により基質であるGM1ガングリオシドが中枢および末梢神経系の細胞、特に神経細胞に異常に蓄積した結果、進行性の神経変性を引き起こす。現在有効な治療法はない。
ムコ多糖症II型など一部のLSDでは欠損した酵素を毎週の点滴で補う酵素補充療法が行われているが、酵素タンパク質は脳のバリア機能である血液脳関門を通過できないため、中枢神経症状には効果が期待できなかった。
近年JCRファーマ社は、ある抗体を融合することで酵素タンパク質が血液脳関門を通過できるJ-Brain Cargo技術を開発した。同技術によりムコ多糖症II型の中枢神経症状を酵素補充療法により改善することが期待されている。
だが、βgalタンパク質の構造が不安定であるためGM1に対する酵素補充療法は存在しない。そこで同研究ではβgalのJ-Brain Cargoを体内で安定的に発現するシステムとして、その発現遺伝子をアデノ随伴ウイルス (AAV)ベクターに搭載し、GM1モデルマウスを用いて遺伝子治療を行った。
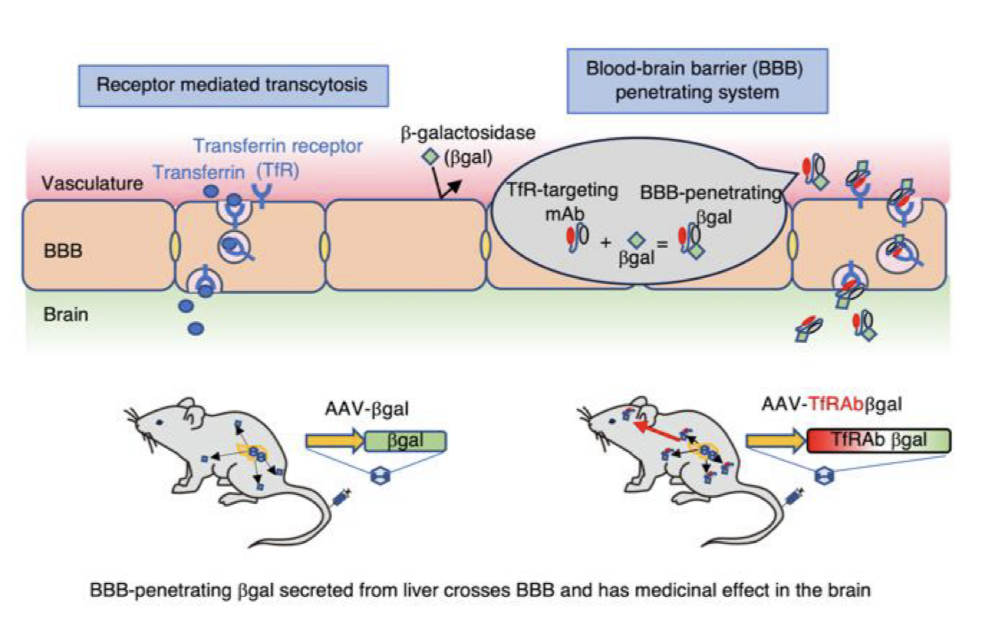
図1. 実験の概要
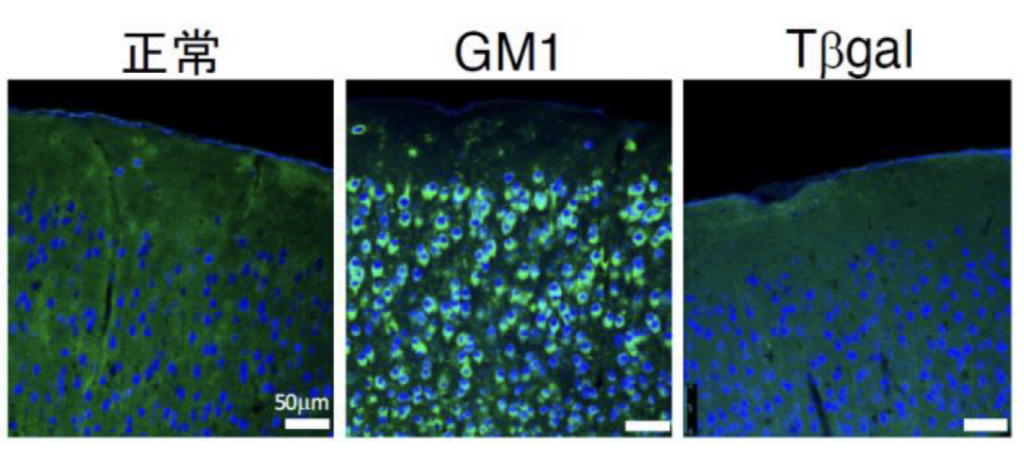
図2. マウス大脳の免疫染色。緑:蓄積物質、青:細胞核。治療により蓄積物質が正常化した。
J-Brain Cargo技術を応用した抗体融合酵素発現遺伝子を搭載したAAV (Tβgal)を10週齢のGM1モデルマウスへ静脈投与し、半年後の脳の酵素活性および蓄積物質の測定による生化学的解析、免疫染色による病理学的解析、複数の行動学的解析を行った。その結果、Tβgal 治療群は生化学的および病理学的解析においてほぼ正常化しており、行動学的解析でも未治療群と比べ有意な改善が認められた。
現在、同研究の臨床応用に向けた検討が進められている。また、同システムは他のライソゾーム病や神経変性疾患への応用が期待される。


