Heartseedは1日、虚血性心疾患に伴う重症心不全を対象とする「他家iPS細胞由来心筋球」 (開発番号: HS-001)について、P1/2試験(LAPiS試験)において、同日、高用量群1例目の安全性評価委員会によるレビューが完了し、高用量群投与の継続が可能となったと発表した。
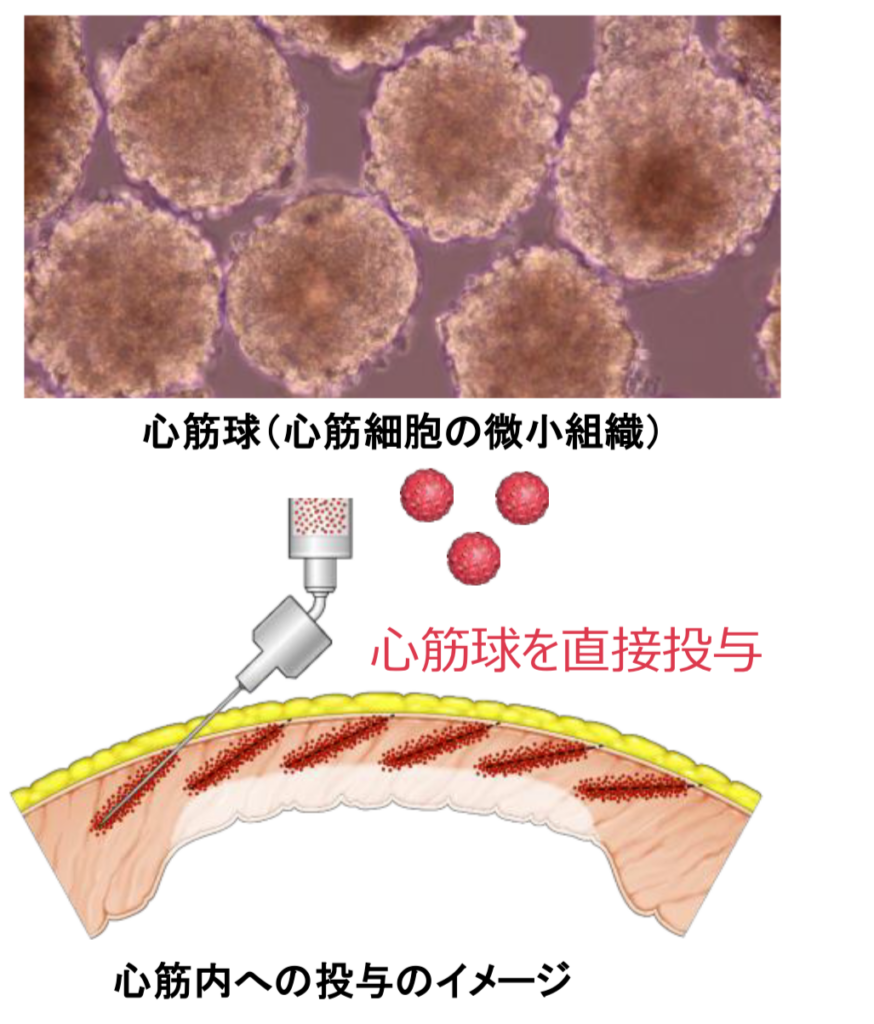
HS-001は、Heartseedの基盤技術に基づいて他家 iPS 細胞由来の純化精製心筋細胞を微小組織(心筋球)にした重症心不全を対象に開発中の再生医療等製品で、Heartseedは、虚血性心疾患による重症心不全を対象とした HS-001の安全性と有効性を評価するLAPiS 試験を国内で進めている。
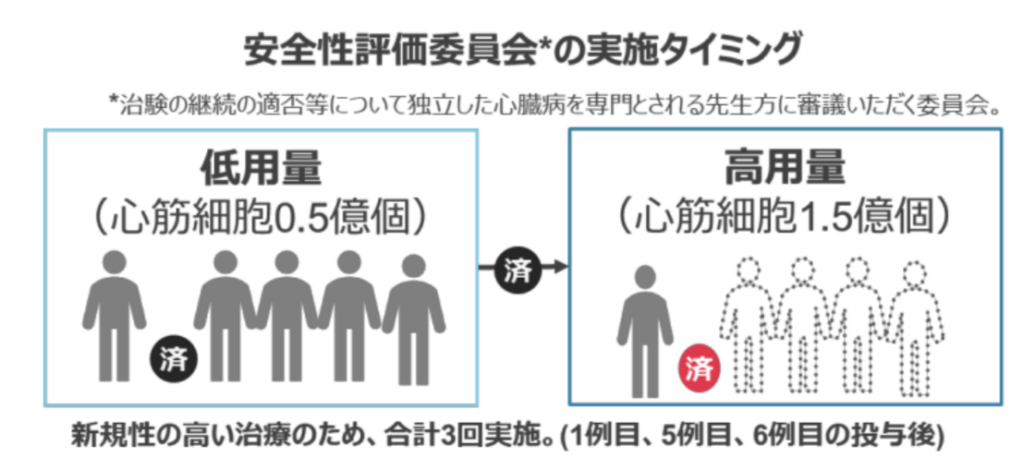
高用量群1例の投与後の経過は順調で、年内に LAPiS 試験 10 例の投与完了を目指す。 LAPiS 試験における低用量群(心筋細胞5千万個)5例への投与結果の安全性については、第2回の安全性評価委員会でレビューされ、高用量群(心筋細胞1億5000万個)への移行が 2024 年7月に推奨されている。これを受けて、同試験高用量群1例目の投与を8月に実施し、第3回の安全性評価委員会で初期安全性が評価され、高用量群の投与を継続していくことが推奨された。
これらの結果からHeartseedでは引き続き高用量群の投与を進め、HS-001の臨床評価を進めていく。なお、LAPiS試験で設定された合計3回の安全性評価委員会は、今回の議論をもって、全て完了した。
◆福田恵一Heartseed代表取締役社長のコメント
1.5億個の心筋細胞を投与する高用量群でも、初期的な安全性が確認できたことを大変うれしく思う。引き続き、LAPiS試験を着実に進めるとともに、高用量群での有効性と安全性に関するデータを収集し、患者さんの治療選択肢の拡大と生活の質の向上に向けて全力を尽くしていく。
◆ Joachim Fruebis Novo Nordisk Cell Therapy R&Dコーポレートバイスプレジデントのコメント
高用量群の投与を進めることが安全性評価委員会で推奨されたことを非常に心強く感じている。これは、重症心不全患者の生活の質を向上させる革新的な治療法開発に向けた我々の取り組みが順調に進んでいることを裏付けるものである。


