浅井ゲルマニウム研究所の研究チームは24日、食品・化粧品原料であるアサイゲルマニウム(有機ゲルマニウム化合物)が、未分化なマクロファージを「M1マクロファージ」へと分化させ、がん細胞に対する攻撃性・貪食能を向上させることを明らかにしたと発表した。同研究成果により、アサイゲルマニウムが新規のマクロファージの分化誘導剤として、新たな免疫療法への応用が期待される。研究のポイントは、次の通り。
① マクロファージをアサイゲルマニウムが含まれる培地で長期間培養することによってM1マクロファージの特徴を持つマクロファージへと分化した。
② アサイゲルマニウムによって分化したマクロファージは「Don’t eat me signal」(SIRP-α CD47 axis)を抑制することにより、がん細胞の認識能・貪食能が高まることが明らかになった。
③ アサイゲルマニウムを長期間摂取したマウスにおいても、腹腔内のM1マクロファージの割合が多く、異物に対する貪食能が亢進していた。
これらの研究成果は、本年1月、査読付き国際科学ジャーナル誌『International Journal of Molecular Sciences』に掲載された。
マクロファージは、「M1マクロファージ」と「M2マクロファージ」の主に2種の活性化マクロファージが存在する。M1マクロファージは、異物に対する認識力・攻撃性が非常に高く、体内でウイルス・細菌の感染細胞や死細胞等を食べることで異物を除去(貪食)し、初期の免疫防御に貢献する。
一方で、M2マクロファージは、M1マクロファージによって生じたダメージを修復する機能や、異物除去の際に生じた炎症を収束させる働きがある。
ヒトの体の中では、一日に数千個のがん細胞ができると言われており、マクロファージをはじめとする主に自然免疫細胞の働きにより、体内にできたがん細胞などの異物を排除し、正常な状態を保っている。特にM1マクロファージは、がん細胞の除去能力が高いことが知られている。過去の研究において、アサイゲルマニウムの抗腫瘍作用を示す結果が得られているが、そのメカニズムは十分にはわかっていなかった。
そこで、同研究は、「マクロファージ」に着目し、アサイゲルマニウムの抗腫瘍作用のメカニズムを明らかにすることを目的として実施された。
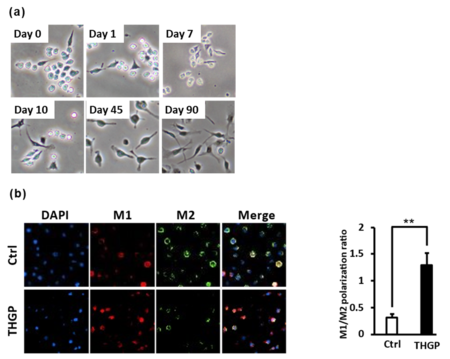
研究では、RAW 264.7細胞 (マウス由来マクロファージ様細胞)をアサイゲルマニウムが含まれる培地で10日間以上培養を行った。
その結果、培養期間に依存して、樹状突起を大きく伸ばした細胞形態へと変化していた (図1a)。
さらに、この細胞を詳細に解析した結果、M1マーカーの発現比が有意に高くなっており、M1マクロファージの割合が増加していることがわかった (図1b)。
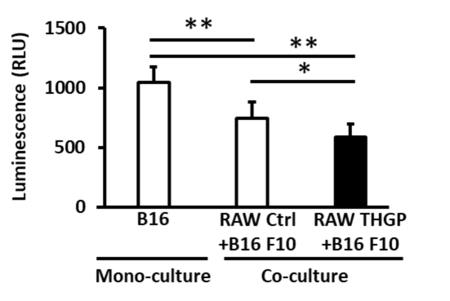
さらに、アサイゲルマニウムによって分化したマクロファージとがん細胞であるマウスメラノーマ細胞(B16)を共培養したとき、コントロールのマクロファージと比較して、マウスメラノーマ細胞に対して高い細胞障害性を示した (図2)。
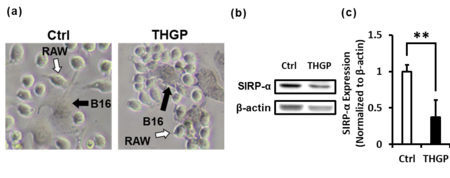
がん細胞は、CD47 という”Don’t eat me signal”を発することが知られている。マクロファージ自身が持つ SIRP-α という認識レセプターでCD47が認識されると、がん細胞を攻撃できなくなってしまう(免疫逃避)。
アサイゲルマニウムによって分化したマクロファージとマウスメラノーマ細胞を共培養したとき、多くのマクロファージがマウスメラノーマ細胞の周辺に集まっていることが確認された (図3a)。
加えて、アサイゲルマニウムによって分化したマクロファージは、SIRP-αの発現が低下しており、がん細胞の認識力が高まっていることが示唆された(図3b, c)。
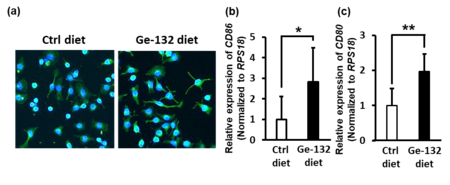
アサイゲルマニウムを30日間摂取させたマウスから腹腔内マクロファージを回収し、マクロファージの形状とM1マーカー(CD86及びCD80)発現の解析を行った。その結果、アサイゲルマニウムを摂取したマウスの腹腔内マクロファージは、樹状突起を伸ばしたものが多数存在していた (図4a)。
このマクロファージのM1マーカーの発現を解析したところ、コントロール食を摂取したマウスよりも、M1マーカーの発現が高いことが確認された (図4b, c)。
近年、がん治療において抗PD-1抗体をはじめとする免疫療法(分子標的薬)が注目を集めている。抗PD-1抗体の標的はT細胞である。
一方、マクロファージを標的とした抗SIRP-α抗体、抗CD47抗体を用いた免疫チェックポイント阻害剤の研究も盛んに行われている。同研究では、アサイゲルマニウムによってマクロファージがM1マクロファージへと分化誘導され、SIRP-αの発現を低下させることを明らかにした。
アサイゲルマニウムによって分化したマクロファージは、がん細胞に対して高い攻撃性を有していることも確認されている。
同研究結果は、アサイゲルマニウムがマクロファージの分化誘導剤として新たな免疫療法につながることが示唆された。
同研究チームでは、今後、ヒト免疫試験を実施し、アサイゲルマニウムのさらなる有効性を確認していく予定である。