MDSの新たな治療戦略への応用に期待
神戸医療産業都市推進機構は、林康貴特任研究員(同構先端医療研究センター血液・腫瘍研究部、日本学術振興会特別研究員SPD)らの研究チームが、骨髄異形成症候群(MDS)由来エクソソームによる骨髄微小環境を介した造血不全の新規メカニズムを解明したことを明らかにした。
MDSは、造血幹細胞移植の適応外となる高齢者が圧倒的多数を占めるため、造血不全に至る原因となるMDS由来エクソソームを制御することで、輸血依存から回避できるなど、今後の新たな治療戦略への応用がが期待される。

同研究成果は、10日に国際科学誌『Cell Reports』にオンライン掲載された。
同研究を実施したのは、井上大地血液・腫瘍研究部長、北村俊雄センター長(研究当時:東京大学医科学研究所(細胞療法分野)教授、現:当機構先端医療研究センター長)らのグループ。


MDSは造血幹細胞レベルでの遺伝子変異を伴う予後不良な悪性腫瘍である。高齢者に多いMDS細胞は、それ自身では弱々しいクローンであり、細胞自律的には増殖することが難しい細胞だ。
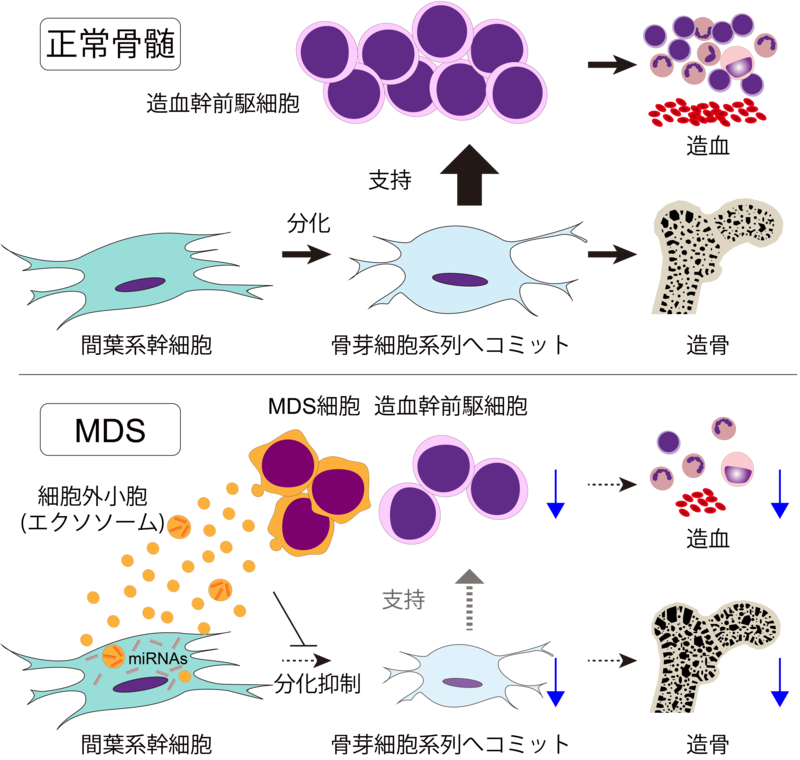
また、MDS患者では骨粗しょう症が多いことが知られている。正常造血細胞は骨芽細胞系列にコミットした間葉系幹細胞によるサポートを受けている(図上)。だが、MDS細胞は細胞外小胞(エクソソーム)を介して、間葉系幹細胞の骨芽細胞系列への分化を抑制し、正常造血への支持力が低下する(図下)。それにより本来は弱々しいはずのMDS細胞が骨髄内でドミナントになり、病期が進展していきます。その副産物として、MDSでは造骨が低下し、骨粗しょう症のリスクが高まる。
MDS患者の骨髄では残存している遺伝子変異をもたない「正常」なはずの造血幹細胞も強く障害を受けていることが判った。だが、その抑制作用は、血球細胞間での直接的な作用ではなく、周囲の支持的ニッチとして重要な間葉系幹細胞を介していた。
MDS細胞は、エクソソームを介して間葉系幹細胞の骨へのコミットメントを阻害し、ヒトでも認められるように骨形成を障害させる。この骨への正常なコミットメントが正常造血に必須であるために、MDS細胞が相対的に優位となり病期が進展していくと考えられる。
さらにMDS細胞が分泌するエクソソーム内のmiRNAが間葉系幹細胞の分化を抑制していることもヒト・マウスの広範な探索から明らかにされた。


