ファンペップは22日、医療法人平心会大阪治験病院で、脊椎関節炎を標的とした抗体誘導ペプチド「FPP003」の医師主導治験(第I相試験)を開始したと発表した。
同治験は、大阪大学大学院医学系研究科が採択された国立研究開発法人日本医療研究開発機構の令和3年度「難治性疾患実用化研究事業(2次公募)/希少難治性疾患に対する画期的な医薬品の実用化に関する研究分野」の研究開発課題「脊椎関節炎を標的とした IL-17Aワクチン(FPP003)の臨床応用」として実施される。
ファンペップは、同研究開発課題について研究開発分担者として参加しており、医師主導治験で使用される治験薬を提供する予定である。
本年12月期に治験薬に関する費用等を計上予定だが、業績に対する影響は軽微である。
大阪大学大学院医学系研究科の中神啓徳寄附講座教授(健康発達医学)、森ノ宮医療大学の冨田哲也教授、大阪治験病院の三上洋病院長らの研究グループは、国立研究開発法人日本医療研究開発機構(AMED)から「難治性疾患実用化研究事業」(2019 年4月から 2021 年3月末の3年間)の支援を受けて脊椎関節炎に対するインターロイキン(IL)-17A を標的とした治療ワクチン(FPP003)の研究開発を進めてきた。
今回、研究グループは、医療法人大阪治験病院にて、抗体誘導ペプチド「FPP003」の医師主導治験(P1試験)を開始した。
FPP003は、幅広い炎症性疾患に関与するタンパク質IL-17Aに対する抗体を誘導するペプチド治療ワクチンで、強直性脊椎炎に代表される体軸性脊椎関節炎の新規治療選択肢となることが期待される。
同治験は、大阪大学が採択された国立研究開発法人日本医療研究開発機構の令和3年度「難治性疾患実用化研究事業(2次公募)/希少難治性疾患に対する画期的な医薬品の実用化に関する研究分野」の研究開発課題「脊椎関節炎を標的とした IL-17A ワクチン(FPP003)の臨床応用」として実施される。
また、同治験で使用される治験薬は、AMED 研究開発課題に研究分担者として参加しているファンペップが提供する。
近年、アルツハイマー病などを標的とした抗体産生を主眼とした治療ワクチンの開発が世界的に行われており、研究グループは、IL-17A を標的としたペプチド治療ワクチン(FPP003)を開発した。
抗 IL-17A 抗体医薬品は、既存治療で効果不十分な尋常性乾癬、関節症性乾癬、膿疱性乾癬に対し治療効果が認められており、本邦でも強直性脊椎炎、X線基準を満たさない体軸性脊椎関節炎に対しても2019-2020 年に3製剤が承認されている。
強直性脊椎炎は、青年期に発症する脊椎と仙腸関節を主な病変部位とする慢性炎症性疾患で、HLAB-27との関連が指摘されているが、病因はいまだに不明で、2015年に指定難病に認定されている。
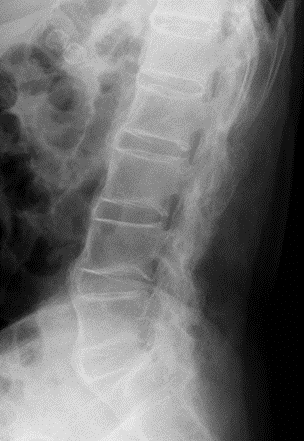
病変部位では、靭帯と骨との付着部位に炎症・骨化(写真)が起こり、疼痛、膨張、運動制限等がみられ、重症例では、体軸関節の強直をきたして日常生活能力の著 しい低下をもたらす。
FPP003が希少疾病である強直性脊椎炎に代表される脊椎関節炎の治療選択肢となることが期待される。
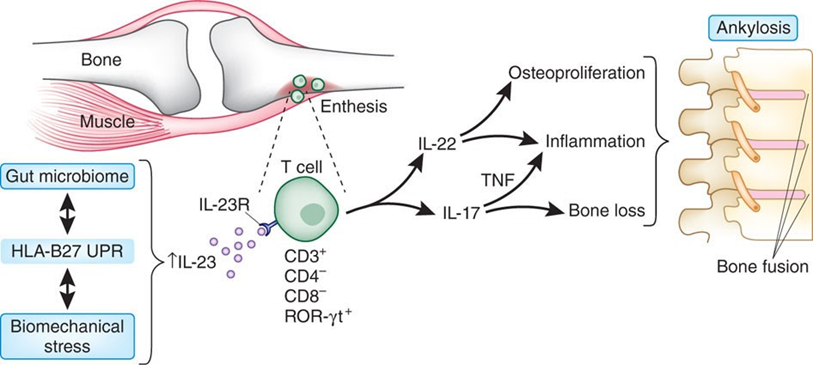
強直性脊椎炎は、仙腸関節炎や脊椎炎による腰背部痛や臀部痛が初発症状となることが多いことが知られている。疼痛が運動により軽快し、安静や就寝により増悪するのが特徴である。アキレス腱の付着部である踵部を初め身体各所の靱帯付着部(関節周辺の骨性突出部など)の炎症徴候(疼痛、腫脹)がしばしば見られ、時に股、膝、肩など四肢の大関節の疼痛や運動制限も生じる。IL-17A は、関節炎に特徴的な付着部炎において重要な役割を果たしていると考えられている。
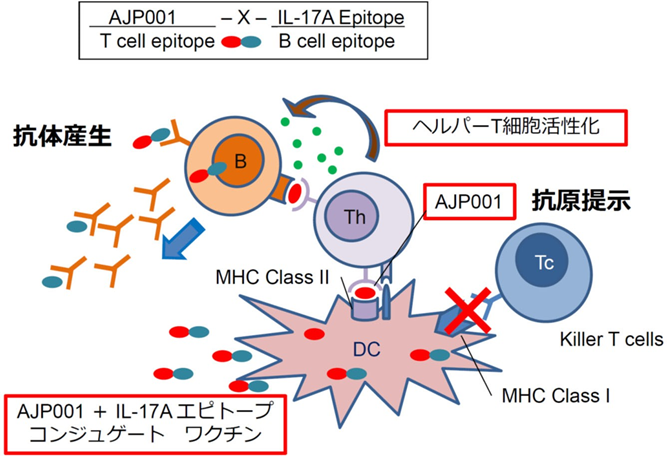
FPP003 は、IL-17A に対する抗体を誘導するペプチド治療ワクチン(抗体誘導ペプチド)である。キャリアペプチド AJP001は、自然免疫活性化作用とキャリアとしての機能を併せ持つ20アミノ酸からなる機能性ペプチドだ。
AJP001とB細胞エピトープを結合させた抗体誘導ペプチドは、樹状細胞に取り込まれて自然免疫活性化作用により樹状細胞を活性化し共刺激分子を発現させる。
また、AJP001 自身がヘルパーT 細胞エピトープとしてヘルパーT細胞に提示され、ヘルパーT細胞を活性化する。AJP001 とB 細胞エピトープを結合させた抗体誘導ペプチドを取り込んだB細胞は、AJP001を提示し、これを認識した活性化T細胞が B細胞を活性化し抗体産生を誘導する。
医師主導治験(第I相試験)の概要は、次の通り。
【研究課題名】 FPP003 の皮下投与時の安全性及び忍容性を評価する単施設無作為化プラセボ対照二重盲
検試験(第 I 相試験)
【目的】 健康成人を対象に FPP003(低用量、高用量)とプラセボを比較し、FPP003 の安全性及び忍容性を評価する。FPP003 は、インターロイキン 17A(IL-17A)に対する抗体を誘導する抗体誘導ペプチ
ド(ペプチド治療ワクチン)であり、FPP003 により産生される抗体を測定して、免疫原性の評価も行う。また、薬物動態の評価も行う。
【目標症例数】FPP003 低用量群:10症例(FPP003 群:8 名、プラセボ群:2 名)
FPP003 高用量群:10 症例(FPP003 群:8 名、プラセボ群:2 名)
【実施期間】2022 年4月~2022年10月
【研究デザイン】単施設、無作為化、プラセボ対照、二重盲検試験
同研究は、日本医療研究開発機構(AMED)難治性疾患実用化研究事業 希少難治性疾患に対する画期的な医薬品及び医療機器、再生医療等製品の実用化に関する研究 薬事承認を目指すシーズ探索研究(ステップ 0)「脊椎関節炎を標的とした IL-17Aワクチンの開発」の支援を受けて行われた。
ファンペップは、2013 年に大阪大学大学院医学系研究科の機能性ペプチドに関する研究成果を実用化する目的で設立された創薬系ベンチャー企業である。
機能性ペプチド「AJP001」を強みとして展開する抗体誘導ペプチドプロジェクト(ペプチド治療ワクチン)と皮膚潰瘍治療薬「SR-0379」を中心に研究開発を進めており、患者のQOL向上へ貢献する医薬品開発による社会貢献を目指している。


