
慢性心不全は、何らかの原因で心機能が低下し、体全体に十分な量の血液を送り出すことができなくなり、息切れやむくみなどの症状が出て、日常生活に支障を来す状態を指す。現在、日本の慢性心不全患者数120万人に上ると推定されている。
高齢化に伴いその数は増加すると考えられているが、慢性心不全の5年生存率は50%と低く、深刻なアンメットニーズが残されている。
こうした中、選択的SGLT2阻害剤「フォシーガ」について、標準治療を受けている慢性心不全に対する効能追加が11月27日に厚生労働省より承認された。
そこで、「慢性心不全の病態と治療における課題」と「慢性心不全におけるフォシーガの期待」を2篇に分けて紹介したい。(アストラゼネカ・小野薬品メディアセミナー、“慢性心不全への新たな治療アプローチ”より)
今後も高齢者心不全患者増加し、心不全治療の課題に
高齢化が進むわが国において、心疾患・脳血管疾患の入院患者は、圧倒的に増え続けている。医療だけでなく、要介護・要支援の原因においても、脳卒中と心臓病が非常に高い。実際に医療費を見ると、脳卒中を含む循環器疾患は平成27年で30兆円に上り、さらに年々増え続けており、脳卒中と循環器疾患で約6兆円の医療費が使われている。これは、がん全体の医療費よりも大きい。こうした背景を踏まえて、平成30年に脳卒中・循環器病対策推進基本法が成立した。本年、それぞれの協議会ができて、実際的な脳卒中・循環器病対策が始まっている。
心不全については、現在120万人ほどの患者がいて、今後も増え続ける傾向にあり、2025年~2030年には130万人に達すると予測される。その後も、人口減少とともに実際の患者数の減少が想定されるが、65歳~74歳、75歳以上の心不全患者は一貫した増加が見込まれている。
この状況予想は、心不全患者は今後も増えていくが、その中で特に高齢の心不全患者が増加することを物語っており、わが国の心不全医療の重要な課題の一つになっている。
特に、わが国の新規の高齢者心不全患者は、2020年から2030年に向けてさらに増え続けると想定されている。2030年には、35万人程度の罹患者の発生が、米国にデーターに基づいて算出されている。
死亡要因としての心不全の割合も増加
心不全の患者数増加に伴い、死亡原因としての心不全の割合も増えている。現時点でわが国の死因の第1位はがんの27.5%、2位が高血圧を除く心疾患で25.3%で、心不全は心疾患による死因の40%を占めている。
また、心疾患の中で最も生命予後が悪いのが心不全と心筋梗塞である。とはいえ、2000年~2018年までの経過を見れば、心筋梗塞の死亡者数は減少傾向にある。その理由は、急性期心筋梗塞に対する急性期の冠動脈インターベーション(PCI)が非常に進歩し、PCIが可能な施設が多くなっているからだ。
一方、心不全も治療自体は進歩しているものの、それ以上に高齢者が増加して実際に心不全で亡くなる患者数が一貫して増加傾向にある。従って、2018年の段階で心疾患の原因別に見た死亡者数では心不全が40%を占め、急性期心筋梗塞は16%で、心不全は心疾患で亡くなる最も多い原因となっている。
2007年から2025年までの関東地区の病院を中心としたトレンドを見ると、心不全で入院した患者の死亡率は8%から低下傾向にある。一方、退院後の1年死亡率は20%で、低下する傾向はみられない。少なくとも院内の死亡率は減少傾向にあるものの、退院後の死亡率は減少していない。
患者自体も2015年までの8年間に高齢化しているので、標準化した死亡率でも低下していない。さらに最も重要なことは、心不全患者は死亡するだけでなく、増悪して再度入院する患者の割合が非常に多いことだ。再入院率は、30日以内でも5%あるが、1年以内では23%と上昇する。
心不全患者は、高齢化していて急性期の治療成績は改善しているものの、長期的には死亡率、再入院率とも改善していないのが、心不全治療のもう一つの課題である。
心不全は増悪を繰り返して重篤化
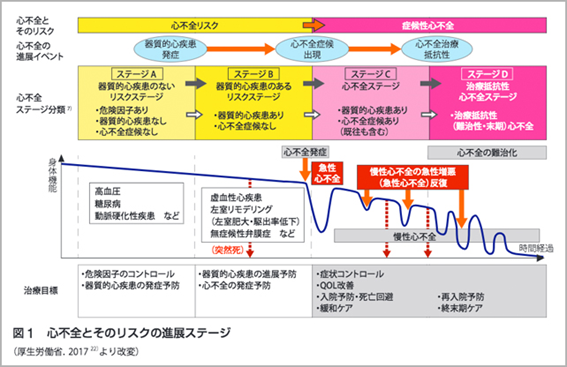
心不全は増悪を繰り返す疾患であり、増悪のたびに新機能は低下してやがて死に至る疾患である。心不全による入院を繰り返すたびに生命予後が不良になり、心不全の増悪が認められた患者は死亡率が高い。
日本循環器学会/日本心不全学会合同ガイドラインでは、心不全の一般向け定義として、「心臓が悪いために、息切れやむくみが起こり、だんだん悪くなり、生命を縮める病気」としている。
心不全とそのリスクの進展ステージでは、高血圧・糖尿病・動脈硬化症などの生活習慣病の段階から「ステージA」として捉えている。ステージAは、心不全ではなく、心不全の兆候もなく、器質的な疾患もない。
虚血性疾患、心筋梗塞、さらには心臓肥大、弁膜症などの器質的疾患が惹起すると「ステージB」になる。このような患者に心不全の症状や兆候が起こってくると「ステージC」に進行し、さらには治療抵抗性の「ステージD」へと移行する。
ステージA~Bには非常に多くの患者がいる。ほとんどの患者は症候が無く、極めて緩徐に進行していく。心不全が発症しても多くの患者は「一旦症状が皆無」になるほど改善するが、増悪を繰り返して進行すれば、だんだんと良い期間が少なくなって悪い期間が多くなり、ステージDへと移行する。このように心不全は、生活習慣病からステージB、C、Dへと一方向性に進行していく。
従って、心不全の治療目的は、各ステージから進行させないことにある。「危険因子をコントロールした生活習慣病に罹患しないようにする」、「生活習慣病の患者は、器質的疾患にならないようにする」、「器質的疾患のある患者は、心不全を発症しないようにする」、「心不全を発症した患者は、増悪を繰り返して入院しないように予防する」ーの4つの段階で予防できる。
実際、ステージC~Dは心不全なので、心不全に対する標準治療のアルゴニズムがガイドラインに示されている。心不全は、左室駆出率で分類する。心臓の左心室が1回駆出することで何%の血液を送り出すことができるかという指標で、正常だと60%あるが、心不全は「40%未満に低下している患者」、「50%以上で駆出率が比較的保たれている患者」、「駆出率40%以上から50%未満の患者」の3つに分類する。
駆出率が低下している患者の標準治療では、ACE阻害薬、ARB、β遮断薬が用いられる。駆出率が保持されている患者は、生命予後を改善する治療が必ずしも明確でないため利尿薬が最も有効であるとされている。
近年、フォシーガなど新規作用機序の心不全治療薬が登場
同ガイドラインは2018年3月に公表されており、一番最後に「今後期待される治療」の章がある。その章には、ガイドラインが公表された時点ではまだ臨床試験が行われていたり、わが国で承認されていないために推奨できない治療薬や治療法で今後に期待できるものが記載されている。
その中にあるIfチャネル阻害薬イバブラジン、アンジオテンシン受容体ネプリライシン阻害薬(ARNI)サクビトリルの2剤は既に承認されている。sGC活性薬ベルイシグアトと、心筋ミオシン活性薬オメカムティブメカルビルは、本年、大規模臨床試験結果が公表され、ポジティブな結果であった。ベルイシグアトは、わが国も含めて承認申請中である。
経皮的僧帽弁接合不全修復システム (マイトラクリップ)は、心不全に対する適応拡大がわが国でも承認されている。
SGLT2阻害薬のフォシーガは、昨年報告されたDAPA-HF試験、今年報告されたEMPEROR-Reduced試験で、いずれも駆出率が保たれら心不全患者を対象に予後を改善したため治療薬として承認されている。 このように、2017年のガイドライン公表から2年間の間に、極めて心不全治療に新しい潮流が訪れており、2021年3月に公表予定の心不全診療ガイドラインフォーカスアップデートに反映される見込みである。
2017年改訂版のアルゴニズムには、Ifチャネル阻害薬イバブラジン、ARNIサクビトリルが追加されており、SGLT2阻害薬の追加もガイドラインの中に位置付けられるものと考えられる。
心不全増悪による再入院防止には患者・家族への教育と福祉との連携が重要
心不全の治療では、再入院の予防は重要で、フォシーガは再入院の予防抑制効果も証明されている。心不全増悪による再入院の誘因を見ると、「塩分・水分制限の不徹底33%」、「治療薬服用の不徹底12%」、「過労11%」、「身体的・精神的ストレス5%」と、治療へのアドヒアランス不良など患者側の要因が多い。
こうした患者側の要因を改善しなければ、どんなに治療薬を開発しても服薬アドヒアランスを高めても、心不全による再入院率は低下しないのは言うまでもない。
さらに、患者側の要因として、「高齢者の独居の増加」、「高齢者同士の介護の増加」も見逃せない。従って、患者側の要因改善には、患者や家族への教育、福祉との連携を念頭に置く必要がある。セルフケア支援は、心不全増悪に対する入院リスクを減少させるデータも報告されている。ガイドラインの中にも疾病管理が記載されており、専門的な教育を受けた医療従事者による患者教育と相談支援が非常に重要になっている。
日本循環器学会では、多職種のアプローチをより円滑にし、心不全に対する疾患管理を向上させる取り組みとして、「心不全療養指導士」の新たな認定制度をスタートした。来年3月には、最初の心不全療養指導士が誕生する。
今後、「心不全療養指導士認定制度」や「脳卒中・循環器病克服5か年計画」などの日本脳脳卒中学会・日本循環器学会の取り組みと、国の「脳卒中・循環器病対策基準法(2019年12月施行)」がリンクする形で、循環器疾患克服への施策がさらに強化されていく。


