アンジェスは13日、バソミューン社共同開発を進めている新型コロナウイルス感染症(COVID-19)治療薬「AV-001」について、米国での臨床試験を開始したと発表した。
AV-001は、アンジェスがカナダのバイオ医薬品企業であるバソミューン社と共同開発を進めているTie2 チロシンキナーゼ受容体アゴニスト。今回、中等度から重度の新型コロナウイルス感染症肺炎患者の治療を目的とした臨床開発について、FDAにIND(新薬臨床試験開始申請)を行い、臨床試験開始許可を得た。
AV-001は、トロントのサニーブルック病院で発見・デザインされ、アンジェスとバソミューン社との共同開発契約に基づき臨床試験を進める。
AV-001の作用メカニズムは、胞表面に最も多く発現する膜貫通型タンパク質であるTie2受容体を標的とした新規治験薬で、Tie2アンジオポエチン経路を活性化させることで、血管機能を正常化させ、血管内皮バリアを回復させるというもの。
新型コロナウイルス感染症および急性呼吸窮迫症候群(ARDS)患者、特に高血圧、糖尿病および肥満などの血管合併症を既往している患者の病態において、血管機能障害が認められる。最近の知見によると、SARS-CoV-2ウイルスが肺内皮細胞に感染して微小血管透過性亢進を引き起こし、血管バリアを変化させ、凝固状態を促進し、血管内皮炎症を誘発し、炎症性細胞の遊走を媒介して、新型コロナウイルス感染症患者における呼吸窮迫と急性呼吸困難症候群(ARDS)を引き起こし、次第に増悪させることが示唆されている。
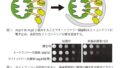
致死性RNA ウイルス感染動物モデルを用いたインフルエンザ/ARDS の前臨床試験において、AV-001は内皮細胞のタイトジャンクションを狭め、血管バリア機能を回復させ、血管透過性亢進をブロックすることで、血管機能を正常化させることが示されている。
AV-001単剤療法では、未治療の対照群と比較して生存期間と肺機能が有意に改善されるが、抗ウイルス療法との併用により有効性はさらに増強されるという利点が示された。AV-001 は、中等度から重度の新型コロナウイルス感染症およびARDS の治療薬として開発されている。
バソミューン社社長兼CEOのダグラス・ハミルトン氏は、「我々は、重症化したSARS-CoV-2 感染患者でみられる過剰な血管透過性亢進の治療を目的とした新規治験薬を開発してきたが、その開発ステージを臨床ステージへと移行させる」と報告。その上で、「このファースト・イン・クラスの治療法が、COVID-19 患者に大きな恩恵をもたらすと期待している」とコメントしている。
一方、アンジェスの山田英社長は、「中等度から重度のCOVID-19肺炎で酸素吸入が行われている入院患者に対する治療法開発は緊急の課題である。前臨床試験成績からみて、本品はその有効な治療法となる可能性がある」と大きな期待を寄せる。
なお、同件の今年度通期連結業績に与える影響は精査中である。