タカラバイオは27日、ウイルス安全性評価試験の受託サービスを日本国内で提供する神戸大学発のスタートアップ企業ViSpot社の子会社化に向け、同社の株式を保有するサンスターと同日付で株式譲渡契約を締結したと発表した。
タカラバイオでは、再生・細胞医療・遺伝子治療薬を中心としたバイオ医薬品の国内最大級の製造施設である遺伝子・細胞プロセッシングセンターを活用し、開発・製造・品質試験について、開発初期フェーズから上市後までワンストップでサポートするCDMO事業を推進している。
ViSpot社のウイルス安全性評価試験受託サービスをタカラバイオのCDMO事業に組み込み、さらに両社のノウハウの相互活用により、新規品質試験メニューの開発加速や効率化、事業領域の拡大といったシナジー効果が期待できる。
これにより、多様なモダリティに対応した品質試験メニューを拡充し、バイオ医薬品の開発・製造・品質試験に関するワンストップサービスをさらに強化し、CDMO事業の拡大を目指す。
ViSpot社は、ウイルス安全性評価試験の課題解決を大きな特徴の一つとする。ウイルス安全性評価試験は、バイオ医薬品が意図せぬウイルスに汚染されていないことを担保するために必須の試験である。製造工程におけるウイルスを除去する能力を評価する「ウイルスクリアランス試験」と、原材料や製品にウイルスが混入していないことを確認する「ウイルス否定試験」が含まれる(図1)。
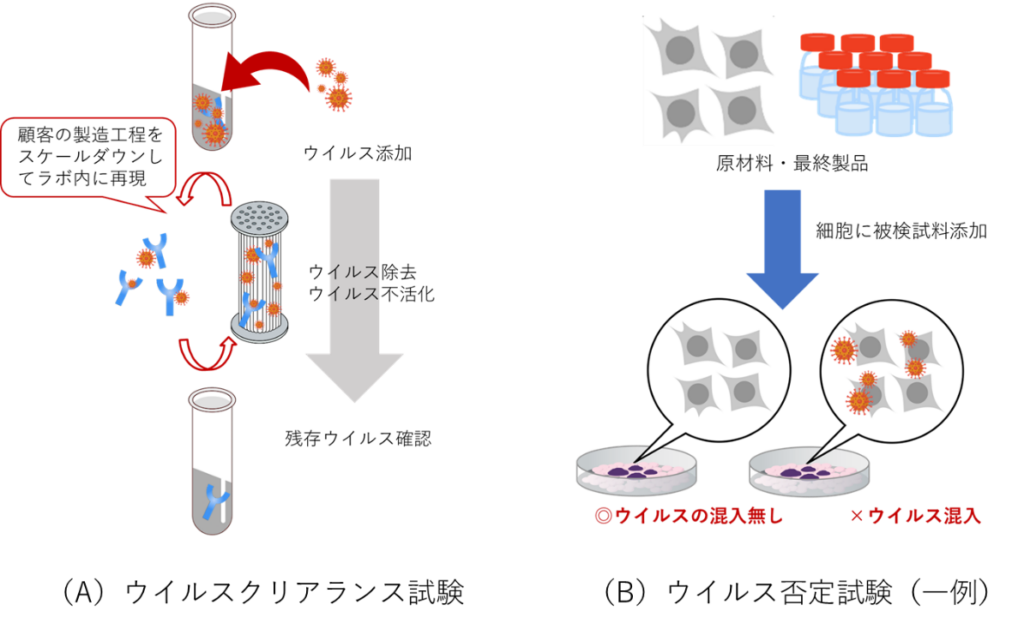
(A)対象とする製造工程にウイルスを添加し、工程前後でウイルスを定量することでウイルス除去能力を評価する試験。(B)原材料や最終製品を指標細胞に添加し、ウイルスが検出されないことでウイルスの混入を否定する試験。
ウイルスクリアランス試験およびウイルス否定試験は、特に、抗体医薬品の開発から上市までのプロセスにおいて必須の試験です(図2)。
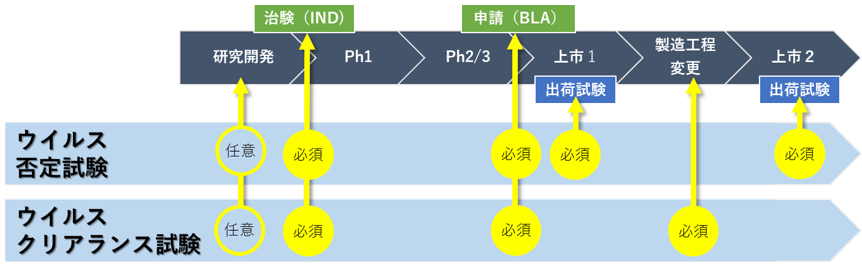
ウイルス安全性評価試験を行う主要な受託試験機関のほとんどが海外に所在しているため、バイオ医薬品を開発する製薬企業は、ウイルスクリアランス試験実施のために開発スタッフを長期にわたって海外に滞在させたりする必要があり、多大な負担となっている。地理的距離の問題に加えて、海外の受託試験機関とのコミュニケーションを円滑に行うハードルは高く、スピード・コスト・利便性の面で、国内のバイオ医薬品開発における長年の課題となっている。
ViSpot社は、このような課題を解決できる数少ない機関の一つだ。日本国内でウイルスクリアランス試験の受託を行う同社は、試験に用いる複数のモデルウイルスの取り扱い技術や、バイオセーフティレベル基準に対応した専用の試験施設に加え、高度な専門知識と経験を有しており、国内のウイルス安全性評価試験のリーディングカンパニーとして、国内の主に抗体医薬品の開発に貢献している。


