脊椎動物は陸上進出によって角層を獲得した

東京工科大学応用生物学部教授の松井毅氏(皮膚進化生物学研究室)は、生物の適応進化をキーワードに皮膚角層バリアの形成メカニズムを研究してきた細胞生物学者だ。
脊椎動物の角層は皮膚の一番外側に死んだ細胞が積み重なることで形成されるが、松井氏らの研究グループはその死に方がアポートーシスでもネクローシスでもない、角層形成時にのみ起こる特殊な細胞死であることを解明し、「コルネオトーシス」という新しい細胞死概念を提唱している。
生物学的な皮膚進化研究を行うようになった理由について、松井氏は「生物の進化で最も大きなイベントは海中で発生した生物たちの陸上進出であり、脊椎動物の場合は気体の中で適応して生きられるように皮膚を獲得した」と話す。さらに、「進化の過程で皮膚がどう変化してきたかを解明すれば、生物の適応進化の謎が解けるのではないか。その最も鍵となる表皮細胞に焦点を絞って研究するようになった」と明かす。
ヒトを含めた現存する陸上脊椎動物(両生類、爬虫類、哺乳類)の表皮細胞の比較や皮膚形成のタイムラプスイメージングなどの手法を駆使して研究を続けてきたという。
松井氏によると、水生生物の魚類やオタマジャクシの皮膚は生きた細胞による多層上皮だが、カエルとして陸上に出たときには未熟ながら死んだ細胞による角層で表皮が覆われるようになった。それが爬虫類では強固な角層に、哺乳類では柔らかく、保湿性の高い角層に進化した(図1)。
また、表面の死んだ細胞の中に多量の水が含まれていること(保湿性)が、哺乳類の角層の特徴だ。
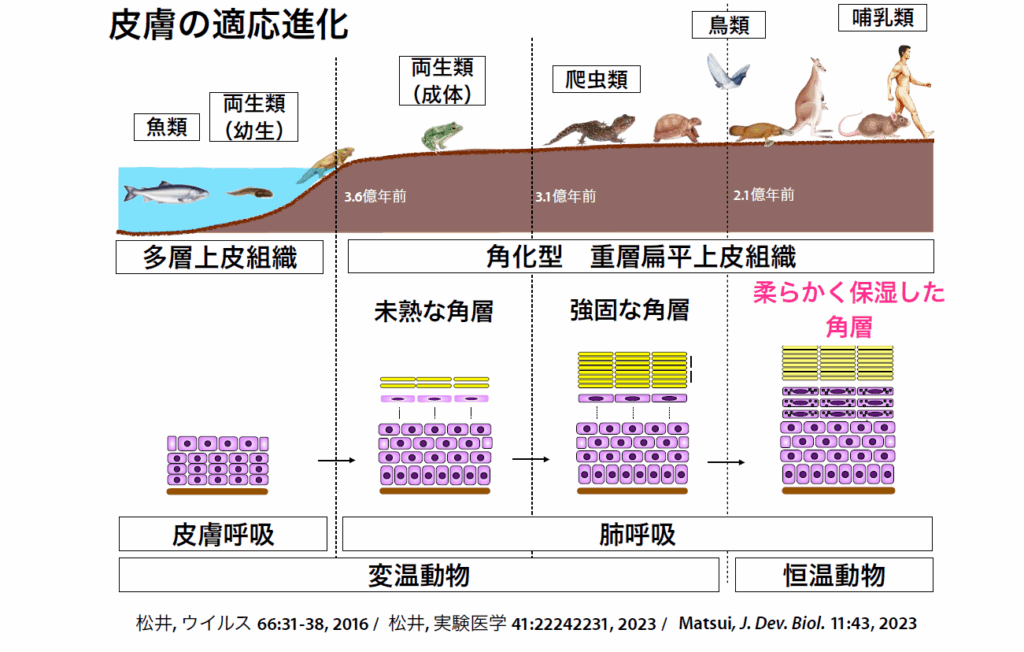
図1 脊椎動物の進化と皮膚の適応進化
松井氏は「角層の形成は、死細胞を使って機能的なマテリアルを作り出すという生体の中では極めてまれな現象」であり、「鍵となるのは、死んだ細胞を作る顆粒層の一番上にある層『SG1細胞』の死に方である」と指摘する。その謎を解くために、松井氏らの研究グループはカエル、ヤモリ、マウス、ヒトなどのSG1細胞の細胞死を詳しく解析してきた。
これまで、SG1細胞が死んで角化する過程では、①細胞死、②細胞小器官分解、③ケラトヒアリン顆粒の分解、④高密度ケラチン形成、⑤コーニファイドエンペローブ形成、⑥角層間脂質形成―という6つの現象が起きることが知られていた。だが、「この中で最初に起きる細胞死のメカニズムは、あまり詳しく分かっていなかった」と明かす。
松井氏の研究成果の一つは、SG1に特異的に発現するSASPase (Skin ASpartic Protease)というレトロウイルス由来酸性プロテアーゼの機能を、2011年に発見したことだ。
ヒトゲノムの中でタンパク質をコードするDNA配列(遺伝子)は2%ほどであり、ゲノムの半分程度を転移因子と呼ばれるDNA配列が占める。転移因子はゲノムの中を動き回る能力を持ち、種が絶滅の危機に瀕するような過酷な環境変化に際して活性化し、ゲノム構造や遺伝子発現を大きく変える役割を担う。転移因子の中にはウイルス様DNA配列を持つものがあり、その一つがSASPaseである。
松井氏が無毛マウスのSASPaseをノックアウトしたマウスを作出すると、顕著な乾燥肌様皮膚を呈した。
また、哺乳類の皮膚表皮細胞に特異的に発現し、皮膚表皮上層では分解されてアミノ酸になることで天然保湿因子を産生するフィラグリン遺伝子の変異がアトピー性皮膚炎の主要な疾患素因であることが知られている。松井氏が作出したSASPaseノックアウト無毛マウスでは異常なフィラグリンの蓄積が観察された。
このことから松井氏は「健常マウスではフィラグリンが分解されて天然保湿成分となるが、SASPaseノックアウト無毛マウスでは異常なフィラグリンが蓄積されることが乾燥肌につながっているのではないか」と考察する。
さらに「SASPaseは哺乳類の祖先から分かれた卵を産む哺乳類(単孔類)であるカモノハシゲノムにもある。進化の過程中で、哺乳類の祖先に突然獲得され活性化したSASPaseが、哺乳類の肌に保湿という機能をもたらしたのではないか」と細胞生物学的仮説を述べる。
SG1細胞のCa2 +濃度の上昇と酸性化が角層形成に重要
続いて、松井氏らは角質形成の初期で起きるSGI細胞が死ぬプロセスを最新のイメージング技術を用いて観察する研究に挑戦した。カルシウムイオン(Ca2+)が結合すると緑の蛍光を発するGCaMP をマウスの皮膚に発現させてタイムラプスイメージングで観察すると、基底層でCa2+濃度が一瞬だけ上昇すること、SG1層でCa2+が約60分間上昇した後、核の凝集、分解が起きることが分かった。
「このとき、SG1層のCa2+濃度の上昇は細胞ごとにバラバラのタイミングで起こる。バラバラのタイミングで細胞が死んで少しずつ表面から剥がれていくので、ムラのない美しい肌ができると考えられる」と説明する。
ただ、GCaMPはpHが低下(酸性化)すると蛍光が消える性質があるため、松井氏らはGCaMP に加えて、pHの影響を受けない赤系蛍光プローブR-CaMPを同時に発現させた追加実験を行った。
すると、GCaMP の緑蛍光は60分を境に急激に下がったが、RCaMP の赤蛍光はその後も発光を続けた。松井氏は「この現象は、SG1細胞が死ぬまではCa2 +濃度が上昇し、死んだ後は細胞内で高いCa2 +濃度が維持されることに加えて酸性化が起きていることを表す」と説明する。
次に松井氏はSG1細胞の酸性化が何をもたらすのかを調べる実験を行った。独自の方法で無毛マウスの顆粒層からSG1細胞だけを分離し、中性から弱酸性の異なるpH溶液で培養してタイムラプスイメージングを行うと、弱酸性溶液のSG1細胞だけで、フィラグリンが凝集したケラトヒアリン顆粒の分解現象が観察された。
他にも、DNAやミトコンドリアの分解も弱酸性にしたときだけにしか起きないことが確認された。このことから「SG1細胞の酸性化が、健常な角層を形成する上で非常に重要であることが分かった」。
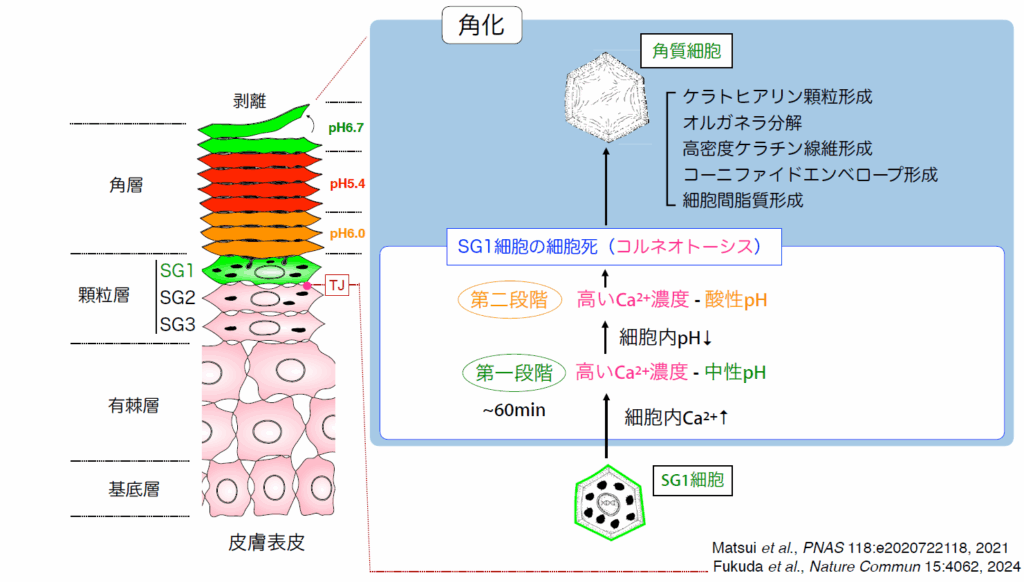
図2 SG1細胞の特殊な細胞死「コルネオトーシス」
これら一連の研究成果から、松井氏らはSG1細胞が死んで角層の機能的バリアを形成するまでの、細胞内の特殊なイオン変化、pH変化を含めたプロセスを「コルネオトーシス(機能的細胞死)」と名付け、新しい概念として提唱している。
松井氏は「酸性プロテアーゼSASPaseの活性化にも酸性化が必要であり、哺乳類に共通する角層の保湿機能の獲得にも酸性化が寄与していると考えられる」と述べる。加えて、「おそらくSG1細胞のCa2+上昇は両生類や爬虫類でも見られるのではないかと推測しているため、それを証明する比較細胞生物学的研究を進めたい。また、われわれの研究成果がアトピー性皮膚炎などの疾患治療や化粧品開発に生かされることを期待したい」と話す。


