Heartseedは、虚血性心疾患に伴う重症心不全を対象とする他家 iPS 細胞由来心筋球 (開発番号: HS-001) のP/12治験 (LAPiS 試験)において、低用量群の安全性評価委員会によるレビューが完了し、高用量群への移行が可能となったことを明らかにした。
HS-001は、Heartseedの基盤技術に基づいて他家iPS細胞由来の純化精製心筋細胞を微小組織(心筋球)にした重症心不全に対して開発中の再生医療等製品で、Heartseedは虚血性心疾患による重症心不全を対象としたHS-001の安全性と有効性を評価するLAPiS 試験を国内で進めている。
LAPiS 試験では、心筋細胞数にして5000万個を投与する低用量群5例への投与が 2024年5月に完了した。用量を規定する毒性や治験の継続に影響を与える安全性上の懸念は見られていない。
安全性評価委員会は、これまでにLAPiS試験で得られている安全性データを評価した結果、心筋細胞数1億5000万個を投与する高用量群へ移行して同試験を継続することを推奨した。
Heartseedでは高用量の投与開始を本年夏以降に予定しており、引き続き HS-001の臨床評価を進めていく。
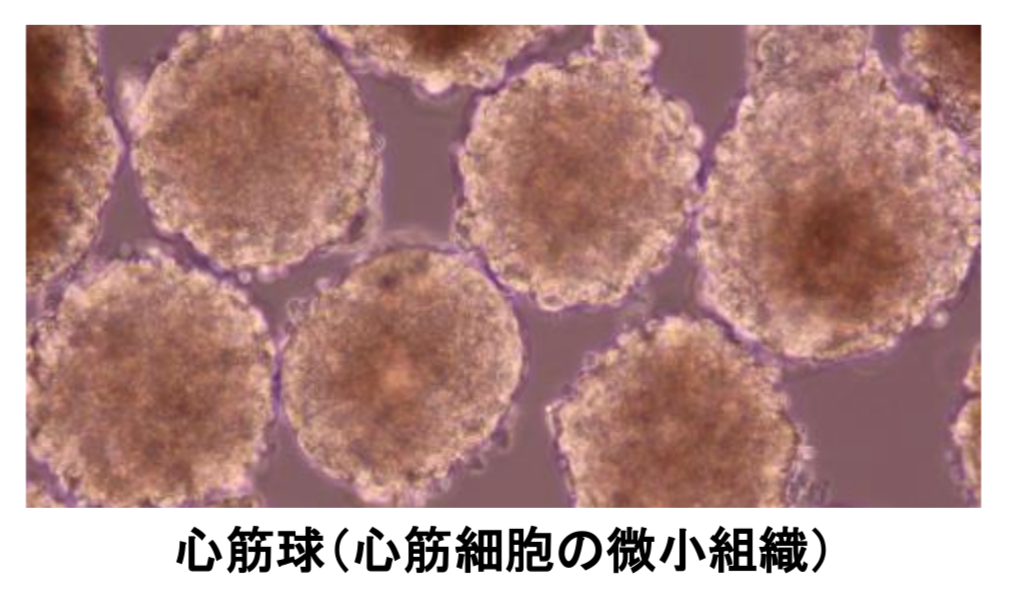
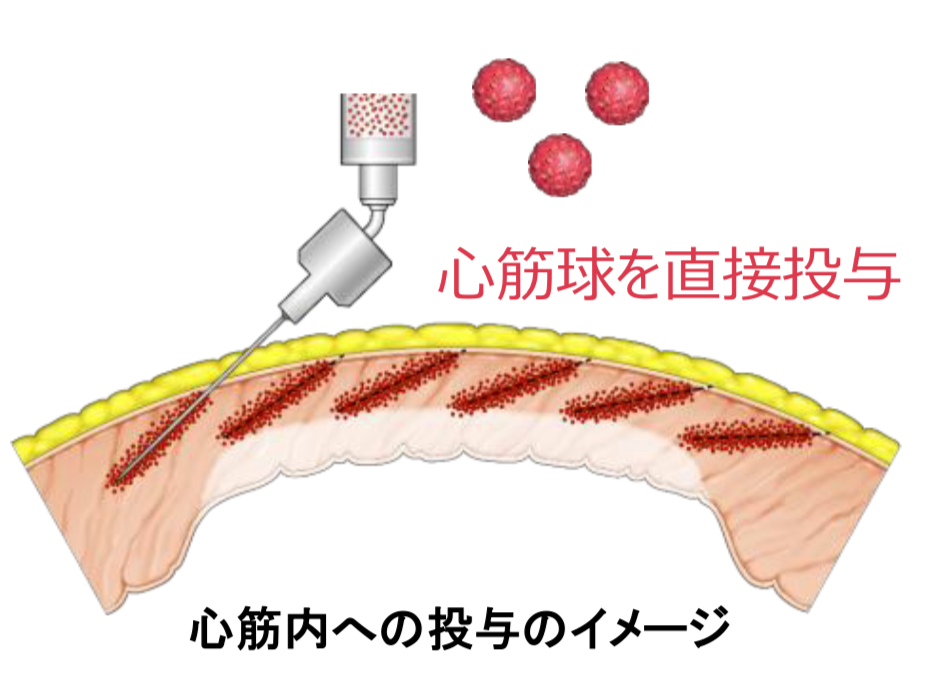
なお、HS-001は、他家iPS細胞から心室筋を高純度で作製し、生着率を高めるために心筋球と呼ぶ微小組織にしたもの。単一細胞と比較して、心筋球にすることで細胞の生着率や生存率が向上することが非臨床試験で確認されている。
心筋球は心臓の心筋層内へ投与することを目的として開発した専用の投与針(SEEDPLANTER)とガイドアダプターを用いて投与する。投与した心筋球は、患者の心筋と結合して再筋肉化することで心収縮力を改善し、また種々の血管新生因子を分泌して投与部位周辺に新たな血管を形成する (neovascularization) という作用機序が期待されている。
LAPiS試験は、虚血性心疾患に伴う重症心不全患者を対象とする52週間のP1/2相多施設共同、非盲検、用量漸増試験である。冠動脈バイパス手術と合わせて、開胸下で専用の投与デバイスを用いてHS-001を心臓の心筋組織内に投与する。予定症例数は10例で、前半の5例には5000 万個、後半の5例には1億5000万個の心筋細胞を投与する。同試験の主要評価項目は投与後26週目の安全性であり、副次的有効性評価項目として、左室駆出率および心筋壁運動評価などを段階的に評価していく。
◆福田恵一Heartseed代表取締役社長のコメント
高用量群投与開始の承認は、HS-001の開発にとって重要なマイルストーンである。これによって、HS-001 の有効性と安全性に関するさらなるデータを収集し、重症心不全患者に新たな希望を提供できることを期待している。
我々の治療法に対して関心を寄せていただいていることをありがたく思っている。LAPiS 試験を着実に進めるとともに、今後も患者様の治療選択肢の拡大と生活の質の向上に向けて全力を尽くしていく。


