岐阜大学大学院共同獣医学研究科の志水泰武教授らの研究グループは、心理的ストレスによって排便が促進される仕組みについて、ストレス中枢から大腸を結ぶ神経伝達路が重要な役割を果たすことを発見した。
ラットを使用した実験により、視床下部―延髄縫線核―脊髄排便中枢―骨盤神経という経路が活性化すると、大腸運動を高めることが分かった。この経路を抑制すると、心理的ストレスによって誘発される排便が減少した。これらの研究成果は、過敏性腸症候群(IBS)などのストレス性排便異常や脳腸相関の理解につながるものと期待される。
これまで、ストレスが排便異常を惹起することは知られていたが、脳のストレス信号がどの経路を通って大腸に伝わるのかは十分に分かっていなかった。
同研究では、ラットを使った実験によって、ストレス中枢として知られる視床下部室傍核(PVH)や視床下部背内側核(DMH)と呼ばれる脳領域から、脳の排便制御領域である延髄縫線核 へストレス信号を伝達する神経経路を発見した。遺伝子技術を使ってこの経路を抑制すると、心理的ストレスによって生じる排便が減弱した。
さらに、この経路の活性化は、脊髄の連絡を介して脊髄排便中枢へと伝わり、骨盤神経を活性化させて排便を起こしていることが明らかになった。
これらの研究成果は、過敏性腸症候群(IBS)などのストレス性排便異常の病態解明や脳腸相関の理解につながると期待される。同研究成果は、4月1日に、Communications Biology誌のオンライン版で発表された。
図
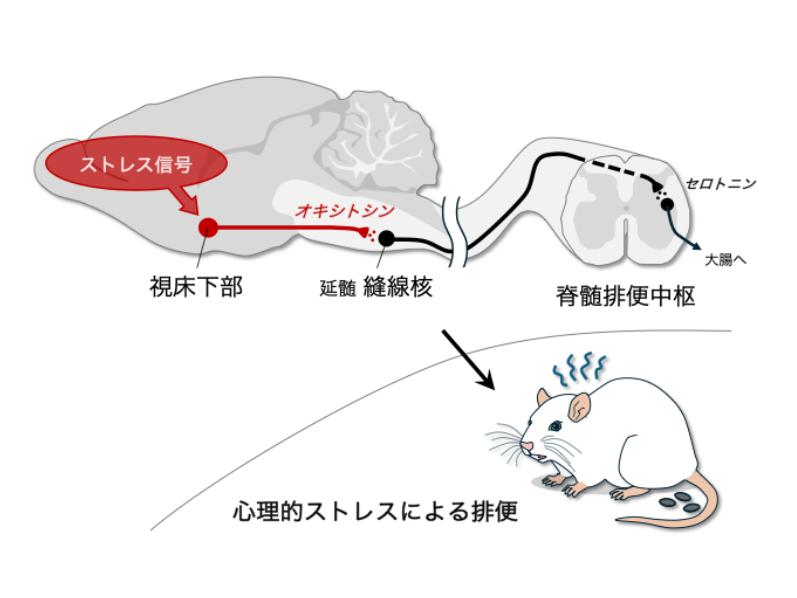
ストレスによって腹痛や下痢、便秘といった症状が生じたり、悪化したりすることはよく知られている。だが、脳で生じたストレス情報が、どのような神経経路を通って大腸に伝わり、排便を変化させるのかは十分に分かっていなかった。同研究は、ラットにおいて心理的ストレスによって起こる排便反応に着目し、その神経回路を明らかにしたもの。
志水氏らは、ラットを水に囲まれた空間に置くことで心理的ストレスを与える「水回避ストレス」と呼ばれるストレス手法を用いて、既知の排便中枢である延髄縫線核へストレス信号を入力する神経経路を探索した。
その結果、視床下部の室傍核(PVH)や背内側視床下部(DMH)と呼ばれる領域から延髄縫線核へ至る神経経路があり、心理ストレスを受けた際に活性化することを明らかにした。
また、麻酔下のラットを用いて大腸運動を測定しながら、これらの視床下部領域を活性化させると、大腸運動の亢進が生じた。これら結果から、PVHやDMHに大腸運動を制御する神経が存在することを明らかにした(図1)。
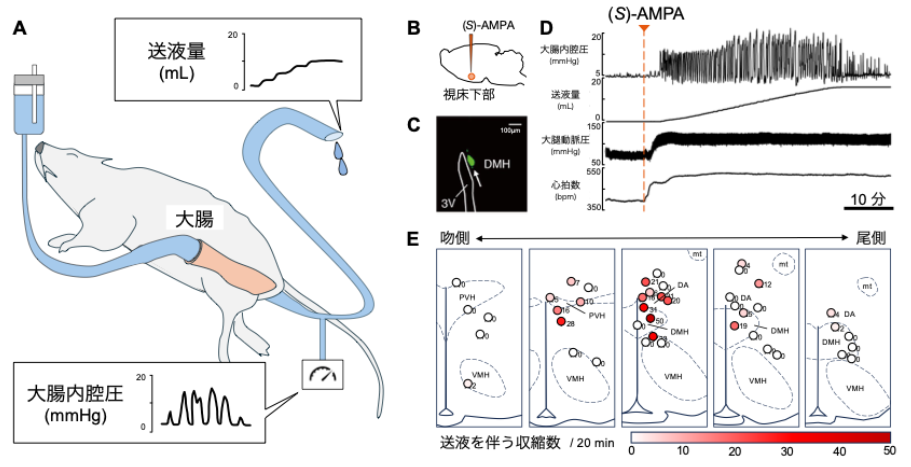
図1 視床下部におけるグルタミン受容体の活性化は大腸運動を亢進する
A:麻酔下のラットを用いて大腸運動を測定する実験。遠位結腸および肛門からカニューレを挿入し、生理食塩水で大腸内腔を満たした。大腸内腔圧と送液量を測定した。B:視床下部に対して (S )-AMPA 注入する実験。C:注入位置は蛍光の粒子(FluoSpheres)により確認された。D:視床下部に(S )-AMPAを注入すると、大腸内腔圧が変動し、内腔を満たす液が送り出される様子が観察された。同時に、動脈圧および心拍数が増加した。E:視床下部の冠状断面図。(S)-AMPA 注入に対する大腸運動応答の強さを赤色の濃淡で示す。丸印は注入部位を示し、隣接する数字は送液を伴う収縮の回数を示す。DMH:視床下部背内側核、3V:第三脳室、PVH:視床下部室傍核、VMH:視床下部腹内側核、DA:視床下部背側野。
そこで、この大腸運動が亢進する応答を起こす経路を確かめるために、脊髄でのセロトニン受容体を遮断する実験や骨盤神経を切断する実験を行ったところ、これらの処置が応答を生じなくさせることを明らかにした。
加えて、延髄縫線核でオキシトシン受容体を遮断すると反応が有意に抑えられ、視床下部由来のオキシトシンによる入力が関与していることが示された。
さらに、化学遺伝学の技術を用いて、PVHやDMHから延髄縫線核へ至る神経経路を選択的に抑制すると、水回避ストレスによって生じる排便が減少した(図2)。
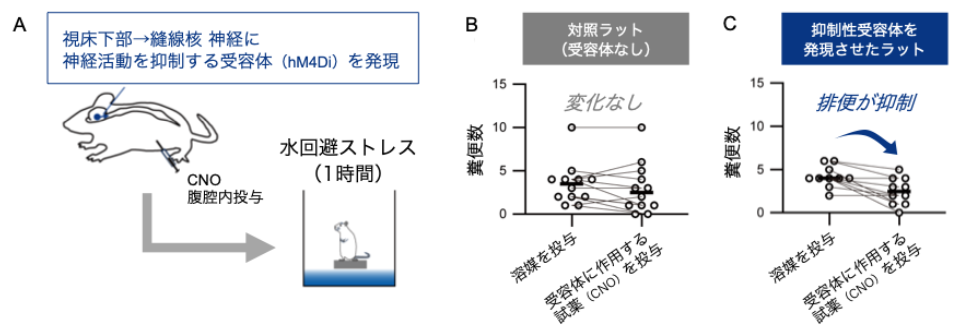
図2 視床下部→縫線核経路の活性化は、心理的ストレスによる排便を引き起こす
A:視床下部から延髄縫線核に投射する神経経路に人工の受容体(mH4Di)を発現させることで神経を抑制する実験。
受容体に作用する試薬(CNO)をあらかじめ投与することで、心理的ストレス(水回避ストレス)による排便が変化するかどうかを検証した。B:対照ラットの排便は変化しなかった。C:神経を抑制したラットでは、排便が抑制された。
これらの結果から、心理的ストレスによる排便には、視床下部―延髄縫線核―脊髄排便中枢―骨盤神経からなる神経経路の活性化が重要であることが明らかになった。
同研究の成果は、一過性の心理的ストレスによって排便が促進される神経回路を示したことだ。今後は、慢性的な心理的ストレスによってこの神経経路にどのような変化が生じるのか、また、その変化が持続的な排便異常にどのように関与するのかを明らかにする必要がある。将来的には、過敏性腸症候群(IBS)など、ストレスに関連する排便異常の病態理解や、新たな治療標的の探索につながることが期待される。
◆研究者コメント
今回明らかにした神経経路の特定はラットを用いた実験の結果であり、ヒトの身体において同様の神経経路が働いているかどうかは、今後更なる研究の積み重ねが必要である。
だが、まだまだ未解明な部分の多いIBSなどの病態を明らかにするためには、まずは基礎研究によって排便を制御する仕組みを解明することが不可欠である。
我々は、基礎研究の知見を少しずつ積み重ねていくことで、患者さんのQOLを著しく低下させる排便異常に立ち向かうための基盤を構築していきたい。


