東京薬科大学・生命科学部・感染制御学研究室の新崎恒平教授らのグループは、感染宿主の自己成分である細胞膜によって覆われたレジオネラ含有液胞膜が細胞内において非自己としてセルオートノマス免疫系に捕捉される仕組みを解明した。
同研究成果は、セルオートノマス免疫系が自己成分を「非自己」として識別できる分子機構の一端を明らかにしたとともに、この仕組みの解析はセルオートノマス免疫系に由来する自己免疫疾患発症機構の理解に繋がるものと期待される。 これらの研究成果は、米国National Academy of Sciencesが刊行する科学誌「Proceedings of the National Academy of Sciences of the United States of America」に掲載された。
免疫系において、「自己」と「非自己」の厳密な識別は必要不可欠だ。一般に、自然免疫系や獲得免疫系では病原体特有の分子パターン(Pathogens Associated Molecular Pattern: PAMP)を基盤として自己と非自己を識別している。
一方、細胞内に侵入した病原体を捕捉し殺傷する『セルオートノマス免疫系』では、自己と非自己の境界が曖昧となっている。その理由として、細胞内に侵入した病原体の多くは剥き出しの状態ではなく、『宿主細胞由来の膜』に覆われて存在しているが、セルオートノマス免疫系では、この宿主由来の膜に覆われた病原体を捕捉し攻撃している。
つまり、「自己由来」の膜成分を「非自己」として認識し攻撃していることから、この識別は病原体のライフサイクルによって引き起こされる宿主因子の分子変動に伴うパターン(Pathogen “Life-cycle” Associated Molecular Pattern: PLAMP)を基盤にしていると考えられる。
それゆえ、細胞内で起こるどのような分子の変化が「自己」を「非自己」としているかを明らかにすることで、セルオートノマス免疫系における『PLAMP』の解明に繋がることが期待される。
レジオネラは、温泉や公衆浴場といった「水」を扱う施設での感染事例を報道などで目にする機会のある病原体で、感染すると重篤な肺炎を引き起こす可能性がある。最近では大阪・関西万博において基準値を超えたレジオネラが検出されたとの報道が記憶に新しい。なお、感染したレジオネラは宿主細胞内において増殖するため、「細胞内発症型細菌」に分類される。
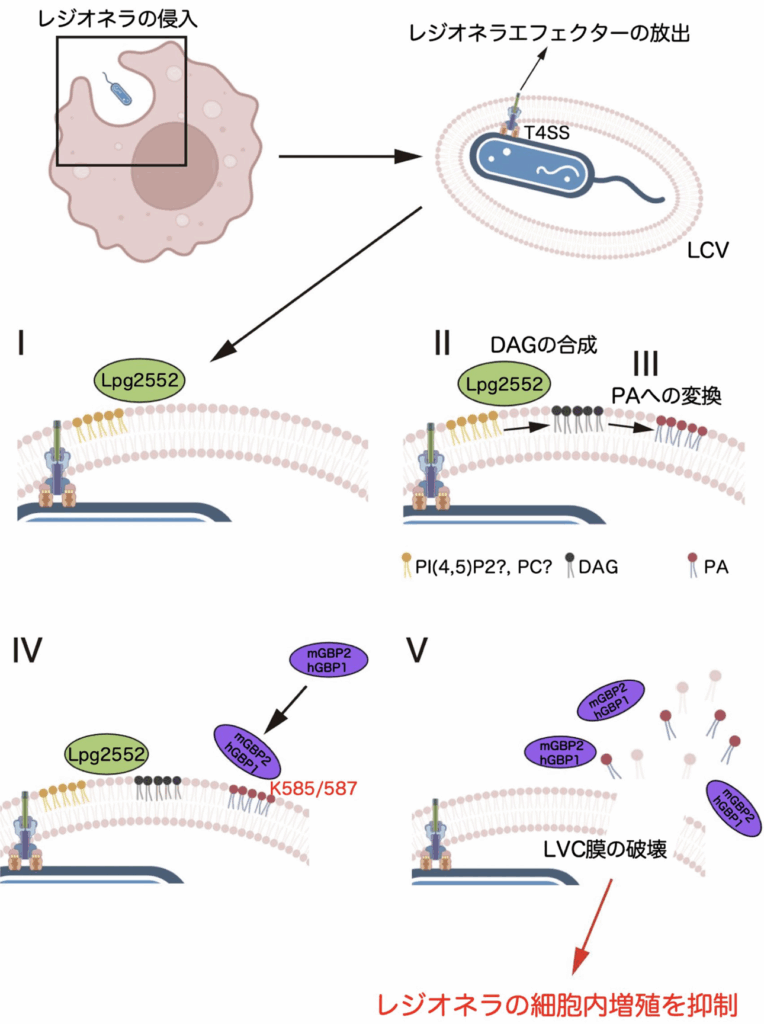
宿主細胞に侵入後、レジオネラはレジオネラ含有液胞(Legionella-containing vacuole; LCV)とよばれる「宿主細胞の細胞膜」によって覆われた膜構造を細胞内に作り出す。その後、レジオネラはLCVの動態を制御することで、LCVのリソソーム(細胞内分解工場)への輸送を遮断するとともに、LCVを自身の増殖の場である小胞体へと誘導する。なお、レジオネラはLCVの動態制御を行うに際して『レジオネラエフェクター』と呼ばれる多くの病原因子を宿主細胞に放出する。
一方で、我々の細胞には細胞内の病原体と対峙できる機構があることが知られている。インターフェロンは感染した病原体に対抗するための遺伝子の発現を亢進するサイトカインの一つであり、先行研究によってインターフェロンで誘導されるGTPaseの一種であるGuanylate binding protein; GBP(マウスにおいてはGBP2・ヒトにおいてはGBP1)はLCV膜を捕捉し破壊することが明らかにされている。
さらに、レジオネラエフェクターが放出できない変異株を含むLCVはこれらのGBPによって捕捉“されない”ことも分かっている。つまり、これらGBPは何らかのレジオネラエフェクターがLCV上で引き起こした分子変動を識別していると推察されるが、その詳細は不明である。
同研究では培養細胞にGBP遺伝子を強制的に発現させるシステムを用い、GBPによるLCVの捕捉を促すレジオネラエフェクターの探索から着手した。
その結果、『Lpg2552』とよばれるレジオネラエフェクターの遺伝子を欠失したレジオネラを含むLCVにおいて、GBPによる捕捉が検出されないことがわかった。Lpg2552はLCV上においてリン脂質のジアシルグリセロール(Diacylglycerol; DAG)の合成を促す因子として報告されていたことから、「GBPはLCV上のDAGを認識する」との仮説を立て検証を行った。
だが、解析の結果、GBPはDAGではなく別のリン脂質であるホスファチジン酸(Phosphatidic Acid; PA)を極めて特異的に認識するという結果が得られた。
この結果は当初の仮説とは異なるように思われるが、細胞内において合成されたDAGは速やかにPAへと変換されることを考慮すると理にかなっている。
実際、PAを特異的に標識する蛍光プローブを用いた解析によりLpg2552依存的にLCV上にPAが蓄積していることを見出した。
これらの結果は、Lpg2552の作用によりLCV上に蓄積したPAをGBPが非自己のサインとして識別していることを示している。通常、PAは細胞小器官といった生体膜の構成成分となる。
そこで、GBPが細胞内においてLCV膜だけを特異的に識別できる(細胞小器官の膜は認識しない)分子機構の解析を行ったところ、GBPが認識できるPAの濃度は通常のPA結合タンパク質が認識できる濃度より極めて高いことを見出した。つまり、GBPはPAの濃度を「自己」と「非自己」の境界線としていると考えられる。
さらに、PAの認識に重要となるGBPのアミノ酸残基(GBP2:585番目のリジン残基・GBP1:587番目のリジン残基)の同定にも成功し、当該残基を変異させたGBPの発現実験により、当該変異はLCVの捕捉やレジオネラの細胞内増殖抑制に極めて大きな影響を与えることが示された。
続いて、Lpg2552によるLCV上でのPA産生がインターフェロン存在下における病原体排除における必要性の検証を行った。まず、インターフェロン処理により発現量が著しく上昇したGBPがLCV膜を捕捉し、未処理の条件と比較してレジオネラの細胞内増殖を強く抑制することを確認した。
一方で、Lpg2552欠損株を含むLCVは、インターフェロンによって発現誘導されたGBPからの捕捉を逃れ、更にはインターフェロン存在下においても有意に増殖していることを発見した。
これらの結果は、セルオートノマス免疫系によるレジオネラの排除にはレジオネラ自身の作用によりLCV上に蓄積したPAが利用されていることを示している。
今回の研究では、セルオートノマス免疫系における「自己」と「非自己」の境界線を決定する分子機構の一端を明らかにすることができた。セルオートノマス免疫系はレジオネラのみならず宿主由来の膜によって覆われた多くの病原体の捕捉と排除に働いていることを鑑みると、今回の研究で明らかにされた知見は、セルオートノマス免疫系による他の病原体捕捉機構の解析の一助になると考察される。
さらには、今回得られた「細胞内のPAの濃度がセルオートノマス免疫系における自己と非自己の境界線になっている」という知見は、GBPに関連した自己免疫疾患の発症機構(当該患者において、異常なPAの蓄積が検出される等)の理解にも役立つと考えられる。