がんなどの治療法開発への応用に期待
東京都立大学理学研究科の廣田耕志教授らの研究グループは6日、世界で初めてゲノム上で細胞内シグナル経路を統合し遺伝子を活性化させる仕組みを発見したと発表した。
今回発見された仕組みは、2つの異なる細胞シグナル伝達経路により支配される転写因子2種が、近接して位置する結合箇所に結合することで相互に安定化し遺伝子を活性化するというもの。今まで未知であった「膨大なゲノム配列から転写因子がどのように結合箇所を見つけるのか」という根源的な謎の一端が解明された。
転写異常は、がんをはじめとする様々な疾患とも関連するため、同研究で明らかになった転写因子結合の新規のメカニズムは、様々な疾患の背後にある原理の理解や治療法の開発につながるものと期待される。
なお、これらの研究成果は6日付け(日本時間)のNucleic acids Researchオンライン版で発表された。
生き物が柔軟に環境に適応するためには外界のシグナルを適切に細胞内に伝達し、環境適応に必要な遺伝子を活性化させることが重要である。遺伝子の活性化は、転写因子が遺伝子の結合箇所へ結合することが契機となって引き起こされる。
だが、ゲノムDNAには、膨大なACGTの塩基配列情報(ヒトでは30億文字)があり、その中からどのようにして転写因子が結合箇所を見つけるのか未解明であった。
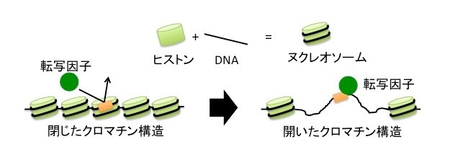
DNAはヒストンと呼ばれるたんぱく質に巻きついてヌクレオソームを形成して核内に収められている(図1)。このヌクレオソームは状況により変化し、ヒストンたんぱく質が外れてDNAがむき出した状態(開いたクロマチン構造)と、きちんとヒストンたんぱく質とDNAが結合した状態(閉じたクロマチン構造)を取ることができ、ゲノムDNAの様々な領域ごとに柔軟に制御されている(図1)。
閉じたクロマチン構造の領域のDNAには転写因子は接近できず結合が阻害されるため、転写因子の結合部位の決定にはクロマチン構造の制御が関わっていることが知られている(図1)。
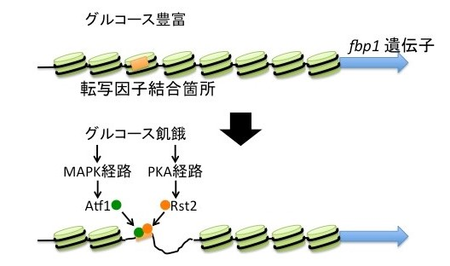
廣田耕志教授らは、分裂酵母をモデル生物に用いてグルコース飢餓ストレスによって転写活性化するfbp1遺伝子のクロマチン制御機構や転写因子の結合に関する解析を行っている。
これまでの研究で、fbp1遺伝子の活性化にはグルコース飢餓ストレスの情報を細胞内にシグナル伝達する経路であるマップキナーゼ(MAPK)経路とプロテインキナーゼA(PKA)経路によりそれぞれ制御されている転写因子のAtf1 とRst2が、fbp1遺伝子の上流部位の近接した箇所に結合することを見出していた(図2)。
だが、これらが近接して結合している意義や結合の仕組みは未解明のままであ
今回、東京都立大学理学研究科の幸田和佳奈大学院生(博士前期2年生、2020年度修了)と千松賢史大学院生(博士後期3年生)は、廣田耕志教授の指導のもと、Atf1とRst2のfbp1遺伝子上流への結合の仕組みについて詳細に解析を行った。
これらの結合部位のクロマチン構造は飢餓ストレスによって開いたクロマチン構造に変化するが、MAPK経路とPKA経路のいずれかのシグナルが不良となると、閉じたクロマチン構造のままとなった。この結果から、2つの経路の両方が同時に活性化することがクロマチンを開く際に必要であることがわかった。Atf1とRst2の結合箇所はACTGの文字数で45文字分しか離れておらず、近接して存在する。この結合箇所において300文字分他のDNA配列を挿入して距離を離すと、Atf1とRst2が同時に結合できなくなるとともに、この領域のクロマチン構造が飢餓ストレスに応答して開かなくなり、閉じたままの状態になった。
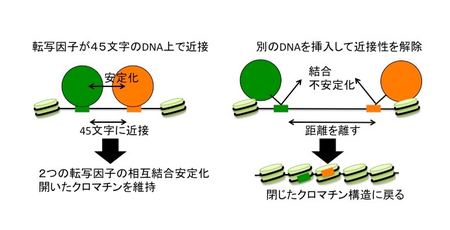
これらは、2つの転写因子が近接した位置で活性化していることで、互いの結合を安定化させるとともに、開いたクロマチン構造を維持させている状態を意味している(図3)。
これらの結果から、転写因子の結合配列が近接して存在することで相互に結合を安定化させ、開いたクロマチン構造を維持させており、そのような転写因子の結合領域はゲノム上でシグナル伝達経路を統合する「ハブ」として機能していると判明した。
外界の環境変動へ適応するために複数のシグナル経路が複雑に相互作用しながら精密に遺伝子を制御するための生命において重要な機構の一端を明らかになった。
今回の研究では、今まで未知であった「膨大なゲノム配列から転写因子がどのように結合箇所を見つけるのか」という根源的な謎の一端を解明した。また、近接した転写因子結合箇所を含むゲノム配列が、シグナル経路を統合させるための「ハブ」として機能できることを見出した。転写異常はガンをはじめとする様々な疾患とも関連するため、同研究で明らかにされた転写因子結合の新規のメカニズムは、様々な疾患の背後にある原理の理解や治療法の開発につながるものと期待される。


