エーザイは12日、同社創製の新薬候補 E7820 について、 国立がん研究センター中央病院および東病院が、固形がんに対する 日本人の安全性および有効性を評価するP1医師主導治験(NCCH2303試験)を開始したと発表した。
同試験は、日本人がん患者由来の腫瘍組織を免疫不全マウスに移植した動物モデルであるJ-PDXの非臨床試験により胆道がんおよび子宮体がんにおける腫瘍縮小効果が確認されたことを受けて実施するもの。
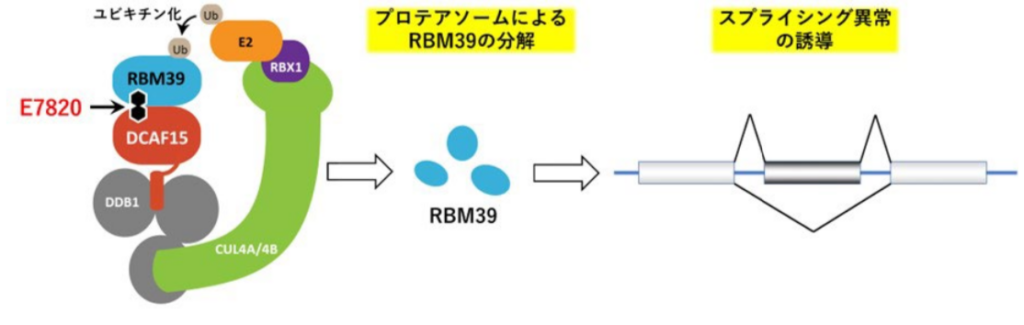
E7820は、選択的なタンパク質分解に関わる DCAF15とスプライシング因子RBM39を結合させる分子糊として作用し、RBM39を選択的に分解するスルホンアミド系抗がん剤である。同作用によってRNAスプライシングの異常が誘導され、がんの増殖を抑える効果が期待される。海外では E7820 を用いた臨床試験の実績がある。
NCCH2303試験において、E7820の忍容性の確認および推奨用法・用量を決定した後、国立がん研究センターとエーザイは、特定のがん種やバイオマーカーを有する固形がんに対する有効性を確認するP3相、さらには承認申請用試験の実施を検討し、薬事承認を目指す。
また、同研究で構築したシステムを、新規抗がん剤開発を加速させる創薬研究システムとして確立する。 エーザイは、国立がん研究センターと新規抗がん剤開発を加速させる創薬研究システム確立を目的に、日本医療研究開発機構(AMED)の医療研究開発革新基盤創成事業(CiCLE)の支援により、「希少がんならびに難治性がんに対する抗がん剤治療開発を加速させる創薬研究手法に関する研究」を2021年より実施している。
同研究において新薬候補E7820は、国立がん研究センター研究所が構築している日本人がん患者由来の腫瘍組織を免疫不全マウスに移植した動物モデルであるJ-PDXのライブラリーを用いて非臨床試験を行い、42 のPDXモデル(膵がん12 モデル、胆道がん12モデル、胃がん9モデル、子宮体がん9モデル)で薬効を評価した。
その結果、E7820 100 mg/kg 投与によって42モデル中16モデル(38.1%)、胆道がんでは12 モデル中7モデル(58.3%)、子宮体がんでは9モデル中5モデル(55.6%)で、腫瘍の縮小が観察された。
PDXモデルは治療効果の予測精度が高く、臨床データとPDXモデルの反応性の間に高い類似性があることから、同研究の結果は胆道がんおよび子宮体がんにおいてE7820の腫瘍縮小効果を示唆している。
さらに、E7820の腫瘍縮小効果と相関するバイオマーカーを探索するため、PDX モデルの全エクソンシークエンスを実施したところ、腫瘍縮小効果が認められたPDXモデルにおいては、BRCA1、BRCA2またはATMといったDNA修復機構の一つである相同組換え修復(HRR)関連遺伝子の変異が高頻度に認められ、当該遺伝子変異が E7820の有効性のバイオマーカーとなる可能性が示唆された。これらの研究成果は、査読付き学術誌「npj Precision Oncology」に掲載された。
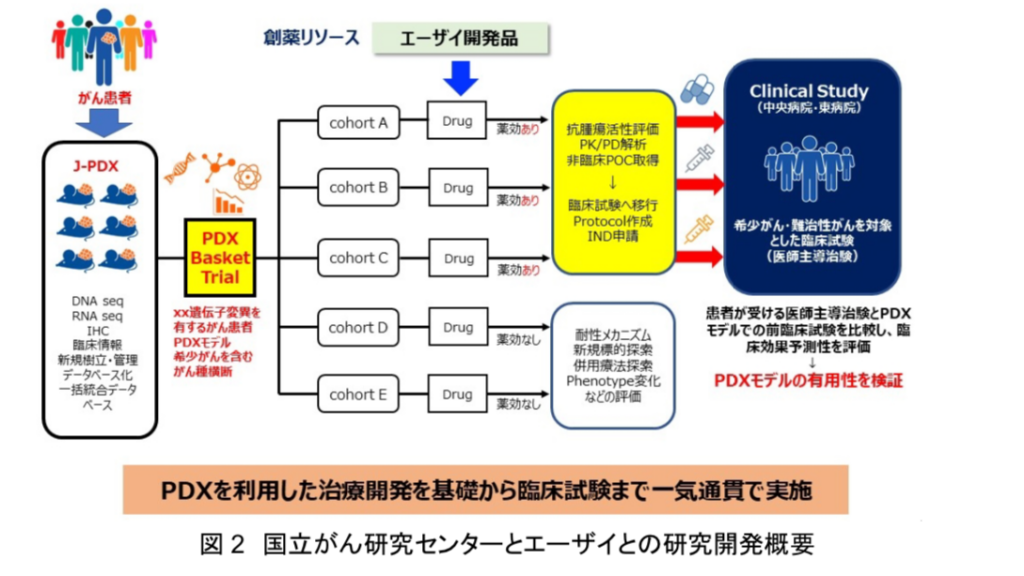
エーザイと国立がん研究センターは、「希少がんならびに難治性がんに対する抗がん剤治療開発を加速させる創薬研究手法に関する研究」において、エーザイ創製の新薬候補品に対して、J-PDX を用いて臓器横断的に非臨床試験を行い、希少がんならびに難治性がんを対象に医師主導治験を実施し、臨床での有用性を確認するとともに、承認申請をめざしている(図 2)。
さらに、治療前後の腫瘍組織からPDXを樹立し、薬剤応答性ならびにがんゲノムの比較解析を行い、新規創薬ターゲットの探索と薬剤耐性機序の解明に取り組み、新たな創薬への展開について検討を進めている。これらの取り組みにより、新規抗がん剤開発を加速させる創薬研究システムの確立を目指す。